Vedoucí: Ing. Petr Bažant, CSc., MBA
E-mail: bazant@biomed.cas.cz | Tel.: +420 296 443 350
Inovační biomedicínské centrum (IBC) napomáhá vzniku a úspěšnému rozběhu spinou firem založených na vědeckých výstupech Ústavu experimentální medicíny. IBC podporuje spolupráci mezi firmami, výzkumnými pracovišti a investory.
Inovační biomedicínské centrum ÚEM je od roku 2008 členem
Společnosti vědeckotechnických parků ČR (www.svtp.cz)
Služby IBC pro inovační začínající firmy jsou orientovány do tří,
navzájem úzce spolupracujících směrů:
Podpora konkurenceschopnosti v biomedicíně – školení v oborech marketing, ochrana duševního vlastnictví, organizace prodeje, management, finanční řízení, sestavení žádosti dotačních projektů, projektový management, právní úkony spojené se založením společnosti, veřejné zakázky a asistence při zavedení systému Správní výrobní praxe. Školení a koučing jsou uspořádány tak, aby začínající firmy překonaly nejčastější úskalí: špatně sestavený business plán a model financování, špatně nastavené vztahy a smlouvy s investorem, špatný management firmy, dodržování korporátních povinností ze zákona a nedostatečné ochrany duševního vlastnictví.
Podpora aplikovaného výzkumu v biomedicíně – certifikované služby v režimu Správné výrobní praxe: testy sterility, výroba odběrových setů, rozplňování, separace a kultivace kmenových buněk apod.
Podnikatelský inkubátor pro spin-off společnosti – služby usídleným firmám: pronájem kanceláří a laboratoří, správa počítačové sítě, řízení nákupu, patentové a daňové služby, skladové hospodářství, recepce, pošta, správa a údržba nemovitosti, prezentace firem, vyhledání investorů a asistence při uzavírání smluv. V současné době je podnikatelský inkubátor plně obsazen.
V současné době jsou v podnikatelském inkubátoru zejména firmy:
Bioinova, s.r.o
vývoj a výroba léčivých přípravků moderní medicíny
Společnost je zaměřena na vývoj a výrobu buněčných léčivých přípravků. V roce 2010 získala povolení k farmaceutické výrobě a v roce 2011 úspěšně prošla periodickým auditem SÚKL, nové povolení k výrobě bylo vydáno v lednu 2012. Bioinova v loňském roce získala povolení ke klinickému hodnocení bezpečnosti a účinnosti pooužití kmenových buněk z kostní dřeně pro léčbu amyotrofické laterální sklerózy. V roce 2012 bylo z plánovaného počtu 10 léčeno prvních 9 pacientů, pro rok 2013 je plánována léčba dalších 10 pacientů. V roce 2012 byla schválena klinická studie ověřující bezpečnost a účinnost kmenových buněk kostní dřeně při zpevnění operované rotátorové manžety. Ředitelem společnosti a vedoucí Oddělení jištění kvality je MUDr. Petr Lesný, vedoucí Skupiny kontrola kvality je RNDr. Kateřina Růžičková, Ph.D, vedoucí výroby je RNDr. Šimona Langkramer-Konrádová a kvalifikovanou osobou je Ing. Ivana Drahorádová. V čistých prostorech pracují zkušené laborantky Jana Tenkrátová a Jana Káclová.
 EponaCell, s.r.o.
EponaCell, s.r.o.
vývoj veterinárních buněčných produktů
Firma se specializuje na aplikaci metod založených na použití kmenových buněk ve veterinární medicíně, zejména u koní a psů. Vybudovala si vlastní laboratorní zázemí s izolátorem pracujícím ve třídě čistoty A na pozadí kontrolované čistoty K. Firma se mimo jiné díky úspěšným tiskovým konferencím velmi rychle prosadila na trhu, má uzavřeny smlouvy s důležitými hráči na trhu veterinární medicíny. EponaCell získala v roce 2012 povolení k výrobě veterinární léčivých přípravků a certifikát výrobce v režimu Správné Výrobní Praxe. V loňském roce bylo léčeno více než 70 zvířecích pacientů. Ředitelem, vedoucím kontroly kvality a minoritním spolumajitelem firmy je Mgr. Daniel Bezděk. Vedoucí výroby je Linda Fedorowiczová a vedoucí jištění kvality je RNDr. Lenka Řeháková. Firma má též svoji kvalifikovanou osobu.
E-mail: daniel.bezdek@eponacell.cz
Tel.: +420 296 943 362
GSM: +420 774 223 233
|
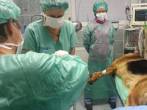
Obr. 1. Anestezie před aplikací kmenových buněk. |
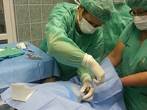
Obr. 2. Aplikace léčebné dávky. |
|
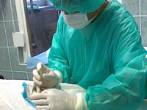
Obr. 3. Aplikace do kolenního kloubu (MVDr. Radek Musil). |
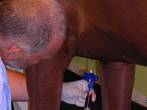
Obr. 4. Odběr kostní dřeně u koně (MVDr. Zdeněk Žert). |
Klinické projekty ÚEM AV ČR
Společně s Centrem diabetologie IKEM od roku 2008 spolupracuje ÚEM na experimentálním posouzení možností využití autologních kmenových buněk kostní dřeně a periferních kmenových (progenitorových) buněk v léčbě ischemické choroby dolních končetin u pacientů se syndromem diabetické nohy. V rámci klinické studie bylo dosud léčeno přes 20 pacientů s diabetem, u kterých byla diagnostikována ischemická choroba dolních končetin se syndromem diabetické nohy.
ÚEM připravuje klinickou studii ověřující bezpečnost a účinnost intrathekálního podání autologních mesenchymálních multipotentních buněk kostní dřeně v léčbě závažného poranění míchy (stupeň A, B nebo C podle ASIA klasifikace).
V roce 2012 byla schválena klinická studie AMSC-ALS-001 ověřující bezpečnost a účinnost intrathekálního podání autologních multipotentních kmenových buněk u pacientů s diagnózou Amyotrofické laterální sklerózy. Studie probíhá ve Fakultní nemocnici Motol a v současnosti v ní je zařazeno již 12 pacientů.
V roce 2013 byla schválena klinická studie AMSC-RC-001, ověřující možnost využití autologních multipotentních kmenových buněk v ortopedii pro urychlení hojení při operaci rotátorové manžety. Studie probíhá ve Fakultní nemocnici Motol.
Úspěšná in vitro a in vivo diferenciace autologních multipotentních kmenových buněk do kostních struktur vedla k podání dvou klinických studií využívající tento mechanismus pro navození synostózy obratlů (AMSC-DSD-001), případně pro hojení rozsáhlých defektů při reimplantaci endoprotézy kyčelního kloubu (AMSC-BDT-001). Obě studie jsou v současnosti schvalovány SÚKL.