Projekty
Mechanismy účinku nukleosidových / nukleotidových analogů a mechanismy vzniku rezistence | |
|
Dlouhodobým cílem projektu je u vybraných cytotoxických látek objasňovat molekulární podstatu jejich antiproliferačních účinků. Základem je popis prostupu látky do buňky, její metabolismus a identifikace účinných metabolitů. Studujeme apoptotické účinky látek a jejich vliv na distribuci buněčného cyklu. Dále sledujeme například vliv látek na proteinkinasovou nebo kaspasovou signalizaci, roli mitochondrií a membránových receptorů a interakce s telomerami / telomerasou. V současné době jsou v hledáčku projektu zejména nové karbocyklické nukleosidy s aktivitou proti některým RNA virům a cytostatickou aktivitou. Znalost metabolismu a mechanismu účinku látek nám pak umožňuje identifikovat potenciální cílová místa vzniku rezistence a navrhnout možná řešení. U rezistentních buněčných kmenů studujeme expresi a funkci membránových přenašečů především ze skupin MDR (P-glykoprotein) a MRP, dále sledujeme fosforylační aktivitu klíčových kinas a citlivost rezistentních kmenů k ostatním běžně používaným cytostatikům (potenciál k navození mnohočetné lékové rezistence). |
Hypometylační účinky látek (epigenetika) | |
|
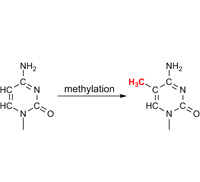
Epigenetika je vědní obor zabývající se změnou chování genů v důsledku chemických změn na povrchu DNA bez změny vlastního genetického kódu (sekvence nukleotidů). Mezi takové změny patří i metylace DNA, kde expresi genů ovlivňuje navázání metylové skupiny na řídící úsek genu. Hypermetylace CpG dinukleotidů ("CpG ostrůvků") tumor-supresorových genů je spojená s jejich inaktivací a může iniciovat vznik nádorového bujení. Jedná se o změny reverzibilní a s využitím látek s hypometylačními účinky je možné hypermetylovaný gen opětovně aktivovat. Tento typ léčby by mohl být u některých specifických (zvláště hematologických) malignit efektivnější a méně toxickou alternativou ke konvenční chemoterapii. V rámci projektu se zabýváme hledáním spolehlivých a účinných metod pro detekci metylované DNA, vyhledáváním nových látek s hypometylačními vlastnostmi a studiem jejich mechanismu účinku. |
Antiangiogenní účinky látek | |

|
Angiogeneze je proces novotvorby krevních cév z existující vaskulatury. Je to komplexní a mnohastupňový proces, na němž se podílí množství mediátorů angiogeneze (složky extracelulární matrix, růstové faktory, integriny, cytokiny a enzymy) s inhibiční nebo naopak stimulační funkci. Dysregulace v procesu angiogeneze zapříčiňují celou řadu patologických stavů jako je např. revmatoidní artritida či diabetická retinopatie. V neposlední řadě je zvýšená angiogeneze nezbytná pro růst solidních tumorů a jejich schopnost metastazovat. Na našem pracovišti se dlouhodobě zabýváme identifikací inhibitorů thymidinfosforylasy (TP), enzymu katalyzujícího fosforolysu thymidinu na thymin a 2-deoxy-D-ribosa-1-fosfát. Angiogenní a antiapoptotické účinky TP (totožné s endoteliálním faktorem PD-ECGF) jsou velmi dobře popsány. Zejména některé nové 5-substituované 6-chlorouracilové deriváty vykázaly na lidské TP izolované z placenty nebo získané rekombinantní technologií významný účinek charakterizovaný inhibičními konstantami v submikromolárních koncentracích (Nencka et al., 2007). Kromě inhibitorů TP se zabýváme i vlivem vybraných látek na některé další angiogenní působky (např. VEGF). V současné době zavádíme nové in vitro modely pro hodnocení antiangiogenních účinků látek na buněčných systémech - konkrétně se jedná o ovlivnění chemotaktického chování vaskulárních endoteliálních buněk (migrace přes mikroporézní membránu) a jejich schopnosti diferencovat za vzniku kapilárních struktur (tzv. tubulogeneze). |
Látky ovlivňující cAMP buněčnou signalizaci | |
|
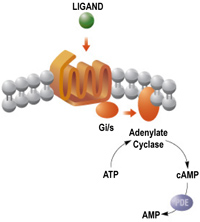
cAMP je derivátem adenosintrifosfátu (ATP) a většina buněk jej využívá jako intracelulárního druhého posla. Jeho vznik z ATP je katalyzován adenylátcyklasami a naopak je rozkládán fosfodiesterasami na 5'-AMP. Dráha adenylátcyklasy sestává obvykle ze tří strukturních částí. První je G-protein, druhou je receptor spřažený s G-proteinem a třetí je samotná katalytická jednotka adenylátcyklasy. Receptory spřažené s G-proteinem představují významný zásahový cíl farmaceutik (40-50% všech používaných léčiv). V naší laboratoři se zabýváme možnostmi ovlivnění hladiny buněčného cAMP novými analogy nukleosidů, nukleotidů a nukleobazí, zejména (ale nejen) cestou inhibice adenylátcyklas - buněčných i exogenních (bakteriálních). Hledáme tak účinné látky s dopady především v terapii některých infekčních a kardiovaskulárních chorob. |
Nové inhibitory xantinoxidasy | |

|
Xantinoxidoreduktasa (XOR) je klíčový enzym katabolismu purinových nukleotidů, který v posledním kroku celého procesu katalyzuje oxidaci hypoxantinu na xantinu a jeho finální oxidaci na kyselinu močovou. Při některých patologických stavech dochází k hromadění kyseliny močové v krevním oběhu (hyperurikémie) a může dojít až k její precipitaci v kloubech a vzniku zánětlivého onemocnění zvaného dna. Jediným lékem používaným v současné době ke korekci hyperurikémie je inhibitor XOR allopurinol. Ten je však poměrně slabým inhibitorem XOR a nebrání zcela produkci kyslíkových radikálů. Na našem pracovišti se zabýváme identifikací nových inhibitorů XOR, které by představovaly výhodnější alternativu k allopurinolu. Ve spolupráci s týmem Strukturní biologie provádíme také kokrystalizace XOR s novými účinnými inhibitory za účelem identifikace vazebného místa inhibitoru a potvrzení mechanismu účinku. |