
Vedoucí:
doc. RNDr. Pavla Jendelová, Ph.D.
E-mail:
pavla.jendelova@iem.cas.cz
Tel.: +420 241 062 828

E-mail:
pavla.jendelova@iem.cas.cz
Tel.: +420 241 062 828
V oddělení jsou studovány mechanismy onemocnění CNS, poranění mozku a míchy a neurodegenerativních onemocnění. Zabýváme se izolací, značením a využitím kmenových buněk a neurálních prekurzorů k léčbě poranění mozku, míchy, Alzheimerovy choroby a amyotrofické laterální sklerózy. Pracujeme s různými typy buněk (mezenchymové kmenové buňky, neurální prekurzorové buňky derivované z linie fetálních spinálních buněk nebo z indukovaných pluripotentních buněk) a přírodními protizánětlivými látkami z hlediska jejich potenciálu napomáhat regeneraci nervové tkáně. Makroporézní polymerní hydrogely jsou využívány jako vhodné nosiče pro růst buněk jak v kulturách in vitro, tak v in vivo implantacích jako cílené nosiče buněk, které podporují regeneraci poraněné tkáně. Cílem buněčné terapie je opravit nebo nahradit, případně zlepšit biologické funkce poškozené nervové tkáně. K zobrazování transplantovaných buněk a jako cílené nosiče pro doručování léčiv využíváme magnetické nanočástice, u kterých testujeme jejich vliv na kmenové buňky i tkáně příjemce.
MUDr. Lucia Urdzíková-Machová, Ph.D.
E-mail: lucia.machova@iem.cas.cz
Tel.: +420 241 062 619
Mgr. Slaven Erceg, Ph.D.
MUDr. Aleš Hejčl, Ph.D.
doc. RNDr. Pavla Jendelová, Ph.D.
Mgr. Kristýna Kárová, Ph.D.
Mgr. Nataliya Romanyuk, Ph.D.
RNDr. Jiří Růžička, Ph.D.
MUDr. Karolína Turnovcová, Ph.D.
MUDr. Lucia Urdzíková-Machová, Ph.D.
Mgr. Ivan Arzhanov
MUDr. Petr Krůpa
Mgr. Dana Mareková
Mgr. Kateřina Neumannová
Mgr. Monika Řehořová
Mgr. Barbora Svobodová
Mgr. Ingrid Vargová
Zuzana Čermáková
Michal Douděra
Karel Třešňák
Alena Veselá
Transplantace neurálních prekursorů derivovaných z fetální tkáně inhibuje NF-kB dráhu a snižuje tak zánětlivou reakci v míšním poranění
Transkripční faktory z rodiny NFκB se podílejí na řadě procesů v průběhu buněčného života. Mezi tyto procesy patří zejména imunitní odpovědi včetně zánětů, buněčné přežívání, růst a vývoj.
V našich projektech jsme se zaměřili na průběh aktivace NFκB po experimentálním kompresním míšním poranění potkana a na to, jak se aktivita změní po transplantaci neurálních prekurzorů (SPC-01) in situ a které mechanismy stojí za funkčním zlepšením, které SPC-01 buňky indukují.
Zjistili jsme, že aktivace NFκB dráhy v prvním měsíci po poranění má dvoufázový charakter s nejvyšší hladinou ve dnech 3 a 28, které odrážejí reakci buněk v místě poškození a také korelují s infiltračními vlnami imunitních buněk z periferie, které byly stanoveny jinými výzkumnými skupinami. Bylo zjištěno, že nejefektivnější v transplantačních terapiích je subakutní podání buněk přibližně 1 týden po poranění. V naší práci ukazujeme, že jedním z důvodů může být i námi pozorované snížení aktivity NFκB právě 7 dní po poranění. Podání kmenových buněk inhibovalo aktivitu prozánětlivé dráhy NF-kB, snížilo hladinu prozánětlivého cytokinu TNF-a a zmírnilo tak rozvoj míšního poranění.
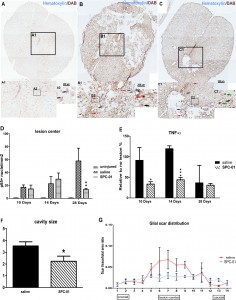
Kmenové buňky blokují aktivaci prozánětlivé dráhy NFkB v míšním poranění
Imunohistochemické barvení hematoxylinem a DAB (NF-kB p65) míchy zdravých potkanů (A, A1, A2) nebo 28 dní po míšním poranění (B, B1, B2) nebo 28 dní po transplantaci kmenovými buňkami (SPC-01; C, C1, C2). Černé šipky ukazují na jádra, která neexprimují NF-kB p65, červené šipky zvýrazňují jádra s translokovaným p65 a zelené šipky označují buňky s jádry negativními na p65 obklopené p65+ cytoplasmou (A1, A2, B1, B2, C1, C2). Ve středu míšní léze byla ve skupině léčené buňkami SPC-01po 28 dnech pozorována signifikantně nižší aktivita NF-kB p65 (D). Ve srovnání s kontrolními zvířaty, transplantace buněk SPC-01 výrazně snížila hladinu TNF-α 10 a 14 dnů po poranění (E). Potkani transplantovaní buňkami SPC-01 vykazovali významně menší velikost léze (F) and menší gliovou jizvu (G) než kontrolní zvířata.
Transplantace kmenových buněk dnes patří mezi terapeutické postupy s významným příslibem multifaktoriálního ovlivnění poškozené tkáně. Kromě přímého nahrazení chybějících buněk a návratu funkce se podílejí na potlačení zánětu, uvolňují četné faktory s regenerativním potenciálem a stimulují sebeobnovující pochody organismu. K detekci transplantovaných buněk se s úspěchem využívá magnetická rezonance, která je neinvazivní, nezatěžuje pacienta ionizujícím zářením, avšak pro dobré zobrazení transplantovaného materiálu je třeba využít kontrastní látku. Využili jsme v našem testu superparamagnetické nanočástice maghemitu (SPION) a částice složené z kobaltu, zinku a železa (CZF), které úspěšně vstupují do buněk přes buněčnou membránu, a hodnotili jejich vliv na oxidativní poškození tkáně po transplantaci do mozku potkana.
Potkaní mesenchymové buňky z kostní dřeně byly označeny in vitro 1) poly-L-lysinem obalenými SPION nebo 2) amorfní silikou obalované CZF a implantovány do levého striata laboratorního potkana. Kontrolní zvířata dostala pouze neznačené buňky. Potkani podstoupili vyšetření pomocí magnetické rezonance. Mozky byly vyňaty po 24 hodinách nebo 4 týdnech od transplantace a v připravené suspenzi z místa transplantace byla hodnocena úroveň oxidativního poškození makromolekul pomocí kometového testu, detekce tvorby karbonylových skupin a 15-F 2t -isoprostanu. U části zvířat bylo provedeno imunohistochemické vyšetření na přítomnost astrogliózy a zánětu.
Magnetická rezonance prokázala přítomnost buněk značených SPION i CZF jako výrazně hyposignálních ložisek. U neznačených buněk je prokazatelné pouze místo podání.
Testy neprokázaly vzestup markerů oxidativního poškození makromolekul (DNA, lipidů a proteinů), stejně tak nedošlo k zánětlivé reakci prokazované přítomností CD68 pozitivních mikroglií, ani k výraznější astroglióze provázené vzestupem pozitivity astrocytárního markeru GFAP.
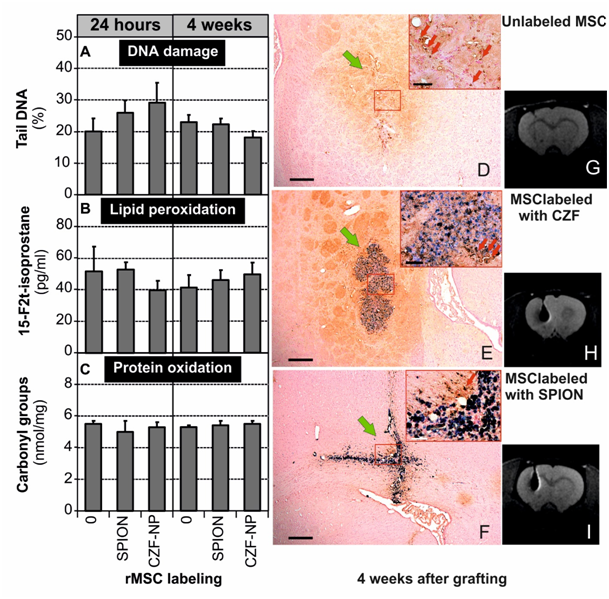
Transplantace magneticky značených buněk do mozku potkana neprokázala žádné poškození makromolekul nervové tkáně (A-C) ani nevyvolala žádnou zánětlivou reakci (D-F). Magneticky značené buňky, na rozdíl od neznačených (G), byly pocelou dobu experimentu dobře viditelné na magnetické rezonanci (H,I).
Publikace: Novotna B, Herynek V, Rossner P Jr, Turnovcova K, Jendelova P.: The effects of grafted mesenchymal stem cells labeled with iron oxide or cobalt-zinc-iron nanoparticles on the biological macromolecules of rat brain tissue extracts. Int J Nanomedicine. 2017 Jun 20;12:4519-4526
Míšní poranění významně ovlivňuje život pacientů po úrazu. Je známo, že epigalokatechin galát – jeden z nejvýznamnějších katechínů zeleného čaje (EGCG), má neuroprotektivní efekt u mnohých neurodegenerativních onemocnění a rovněž po poranění CNS. Cílem našeho výzkumu bylo objasnit, jakou roli hraje EGCG aplikovaný potkanům s míšním poraněním. EGCG jsme podávali ihned po míšním poranění a pak následujících 28 dnů v celkové i místní aplikaci. Sledovali jsme množství zachovalé bílé a šedé hmoty, růst axonů, zlepšení neurologického deficitu zvířat a tvorbu gliové jizvy. Podání EGCG zlepšilo motorické funkce a zvýšilo počet nových axonů v místě poranění. Rovněž došlo ke změnám ve vylučování zánětlivých cytokínů (redukce IL-6, IL2, MIP1α and RANTES a zvýšená exprese IL-4, IL-12p70 and TNFα) a byla výrazně snížena translokace NF-κB do jádra. Zvýšená byla i exprese růstových faktorů (FGF2 a VEGF) v míšní tkáni.
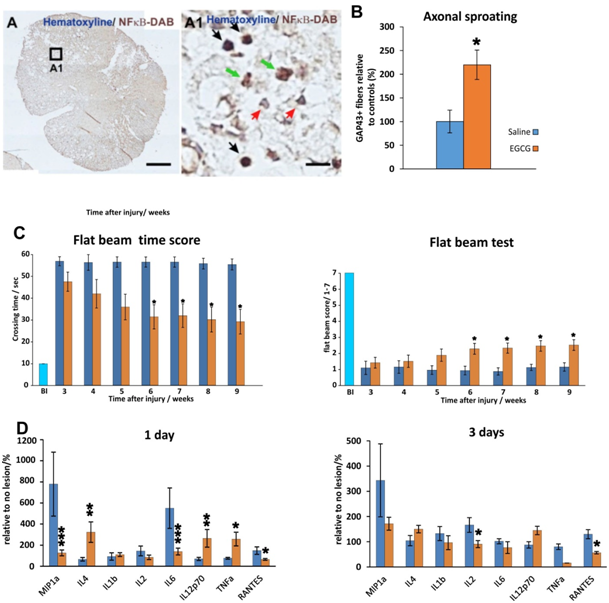
Na obrázku je znázorněna zvýšená jaderná translokace podjednotky p65 (RelA) NF-κB dimeru po podání EGCG (černá šipka). měřítko A = 500 μm, A1 = 20 μm. Nárůst počtu regenerujících axonů po aplikaci EGCG (B). Motorické zlepšení bylo pozorováno u potkanů léčených EGCG během chůze po kladině (C). Změny zánětlivých cytokínů jeden den a tři dny po míšním poranění (D).
V naší studii jsme porovnávali vliv třech různých typů kmenových buněk, připravených z různých zdrojů, na regeneraci nervové tkáně po míšním poranění u potkana. Použili jsme lidské mezenchymové kmenové buňky, izolované z kostní dřeně, které nejsou neurálního původu, ale jsou často využívány v klinických studiích, linii spinálních progenitorových buněk získaných z 10 denního lidského plodu a neurální prekurzory z indukovaných pluripotentních buněk (iPSC). V modelu kompresního míšního poranění potkana jsme sledovali přežívání a diferenciaci buněk, změny neurologického deficitu a molekulární a strukturální změny tkáně příjemce. Oba typy neurálních prekurzorů přežívaly velmi dobře po celou dobu studie. Spinální progenitorové buňky diferencovaly především do astrocytů a v menší míře do oligodendrocytů a neuronů. Oproti tomu neurální prekkurzory z iPSC diferencovaly převážně do neuronů a jen v menší míře do astrocytů. Všechny tři typy buněk výrazně zlepšily lokomoční deficit po míšním poškození. Nejvýraznější pozitivní změny byly pozorovány po aplikaci neurálních prekurzorů z iPSC. Tento efekt byl podpořen zejména jejich schopností podpory zachování míšní tkáně či růstu axonů v poškozené míše.
Zatímco buňky neurálního původu aplikované do tkáně velmi dobře přežívaly v poraněné míše po dobu 2 měsíců, mezenchymové kmenové buňky kostní dřeně aplikované intrathekálně byly nalezeny jen na povrchu míchy 14 dní po aplikaci. Oba typy neurálních prekurzorů diferencovaly do astrocytů, oligodendrocytů a neuronů. Aplikace všech 3 typů buněk zlepšila motorické schopnosti experimentálních zvířat. Neurální prekurzory z iPSC měly nejvíce protektivní účinek v oblasti šedé hmoty a podpořily růst axonů v místě poranění.
Publikace:
Ruzicka J, Machova-Urdzikova L, Gillick J, Amemori T, Romanyuk N, Karova K, Zaviskova K, Dubisova J, Kubinova S, Murali R, Sykova E, Jhanwar-Uniyal M, Jendelova P. A Comparative Study of Three Different Types of Stem Cells for Treatment of Rat Spinal Cord Injury. Cell Transplant. 2017 Apr 13;26(4):585-603. Epub 2016 Nov 2.
2018
Ruzicka J, Urdzikova LM, Kloudova A, Amin AG, Vallova J, Kubinova S, Schmidt MH, Jhanwar-Uniyal M, Jendelova P. Anti-inflammatory compound curcumin and mesenchymal stem cells in the treatment of spinal cord injury in rats. Acta Neurobiol Exp (Wars). 2018;78(4):358-374.
Artero-Castro A, Popelka S, Jendelova P, Motlik J, Ardan T, Rodriguez Jimenez FJ, Erceg S. The identification of small molecules that stimulate retinal pigment epithelial cells: potential novel therapeutic options for treating retinopathies. Expert Opin Drug Discov. 2019 Jan 8:1-9. doi: 10.1080/17460441.2019.1559148.
Plichta Z, Kozak Y, Panchuk R, Sokolova V, Epple M, Kobylinska L, Jendelová P, Horák D. Cytotoxicity of doxorubicin-conjugated poly[N-(2-hydroxypropyl)methacrylamide]-modified γ-Fe(2)O(3) nanoparticles towards human tumor cells. Beilstein J Nanotechnol. 2018 Sep 25;9:2533-2545. doi: 10.3762/bjnano.9.236.
Jendelova P, Sykova E, Erceg S. Neural Stem Cells Derived from Human-Induced Pluripotent Stem Cells and Their Use in Models of CNS Injury. Results Probl Cell Differ. 2018;66:89-102. doi: 10.1007/978-3-319-93485-3_3.
Hejčl A, Růžička J, Kekulová K, Svobodová B, Proks V, Macková H, Jiránková K, Kárová K, Machová Urdziková L, Kubinová Š, Cihlář J, Horák D, Jendelová P. Modified Methacrylate Hydrogels Improve Tissue Repair after Spinal Cord Injury. Int J Mol Sci. 2018 Aug 22;19(9). pii: E2481. doi: 10.3390/ijms19092481.
Hejčl A, Růžička J, Proks V, Macková H, Kubinová Š, Tukmachev D, Cihlář J, Horák D, Jendelová P. Dynamics of tissue ingrowth in SIKVAV-modified highly superporous PHEMA scaffolds with oriented pores after bridging a spinal cord transection. J Mater Sci Mater Med. 2018 Jun 25;29(7):89. doi: 10.1007/s10856-018-6100-2.
Krupa P, Vackova I, Ruzicka J, Zaviskova K, Dubisova J, Koci Z, Turnovcova K, Urdzikova LM, Kubinova S, Rehak S, Jendelova P. The Effect of Human Mesenchymal Stem Cells Derived from Wharton's Jelly in Spinal Cord Injury Treatment Is Dose-Dependent and Can Be Facilitated by Repeated Application. Int J Mol Sci. 2018 May 17;19(5). pii: E1503. doi: 10.3390/ijms19051503.
Bolinches-Amorós A, Lukovic D, Castro AA, León M, Kamenarova K, Kaneva R, Jendelova P, Blanco-Kelly F, Ayuso C, Cortón M, Erceg S. Generation of a human iPSC line from a patient with congenital glaucoma caused by mutation in CYP1B1 gene. Stem Cell Res. 2018 Apr;28:96-99. doi: 10.1016/j.scr.2018.01.004.
Ruzicka J, Urdzikova LM, Svobodova B, Amin AG, Karova K, Dubisova J, Zaviskova K, Kubinova S, Schmidt M, Jhanwar-Uniyal M, Jendelova P. Does combined therapy of curcumin and epigallocatechin gallate have a synergistic neuroprotective effect against spinal cord injury? Neural Regen Res. 2018 Jan;13(1):119-127. doi: 10.4103/1673-5374.224379.
Artero Castro A, Lukovic D, Jendelova P, Erceg S. Concise Review: Human Induced Pluripotent Stem Cell Models of Retinitis Pigmentosa. Stem Cells. 2018 Apr;36(4):474-481. doi: 10.1002/stem.2783. Epub 2018 Feb 7. Review.
Karova, K., Wainwright, J.V, Machova-Urdzikova, L., Rishikaysh Pisal, R.V., Schmidt, M., Jendelova, P., Jhanwar-Uniyal, M. Transplantation of neural precursors generated from spinal progenitor cells reduces inflammation in spinal cord injury via NF-κB pathway inhibition. J Neuroinflammation in press doi: 10.1186/s12974-019-1394-7.
Jiri Ruzicka, J.,Romanyuk, N., Jiráková, K. Hejcl, A., Janoušková, O., Urdzikova Machova, L., Bochin, M., Pradny, M., Vargova, L., Jendelova, P. The effect of iPS derived neural progenitors seeded on laminin coated pHEMA-MOETACl hydrogel with dual porosity, in a rat model of chronic spinal cord injury Cell Transplantation in press. Doi: 10.1177/0963689718823705.
Forostyak, S. , Syková, E.: (2017) Neuroprotective Potential of Cell-Based Therapies in ALS:From BenchtoBedside. Frontiers in Neuroscience. 11: 591.
Hejčl, A. , Vondráková, K., Kelbich, P., Sameš, M., Tsenov, G., Kačer, P.: (2017) Model cerebrálních vazospasmů a metabolomické mapování. (A Model of Cerebral Vasospasms and Metabolomic Mapping.) Chemické listy. 111(1): 56-61.
Herynek, V., Gálisová, A., Srinivas, M., van Dinther, E.A.W., Kosinová, E., Růžička, J., Jirátová, K., Kříž, J., Jirák, D.: (2017) Pre-Microporation Improves Outcome of Pancreatic Islet Labelling for Optical and F-19 MR Imaging. Biological Procedures Online. 19: 6.
Kaman, O., Dědourková, T., Koktan, J., Kuličková, J., Maryško, M., Veverka, P., Havelek, R., Královec, K., Turnovcová, K., Jendelová, P., Schröfel, A., Svoboda, L.: (2016) Silica-coated manganite and Mn-based ferrite nanoparticles: a comparative study focused on cytotoxicity. Journal of Nanoparticle Research. 18(4): 1-18, č. článku 100.
Kočí, Z., Výborný, K., Dubišová, J., Vacková, I. , Jäger, A., Lunov, O., Jiráková, K., Kubinová, Š.: (2017) Extracellular Matrix Hydrogel Derived from Human Umbilical Cord as a Scaffold for Neural Tissue Repair and Its Comparison with Extracellular Matrix from Porcine Tissues. Tissue Engineering part C- Methods. 23(6): 333-345.
Lukovic, D., Diez Lloret, A., Stojkovic, P., Rodríguez-Martínez, D., Arago, M.P.P., Rodriguez-Jiménez, F.J., González-Rodríguez, P., López-Barneo, J., Syková, E., Jendelová, P., Kostic, J., Moreno-Manzano, V., Stojkovic, M., Bhattacharya, S.S., Erceg, S.: (2017) Highly Efficient Neural Conversion of Human Pluripotent Stem Cells in Adherent and Animal-Free Conditions. Stem Cells Translational Medicine. 6(4): 1217-1226.
Lukovic, D., Moreno-Manzano, V., Rodriguez-Jimenez, F.J., Vilches, A., Syková, E., Jendelová, P., Stojkovic, M., Erceg S.: (2017) HiPSC Disease Modeling of Rare Hereditary Cerebellar Ataxias: Opportunities and Future Challenges. Neuroscientist. 23(5): 554-566.
Machová-Urdzíková, L., Růžička, J., Kárová, K., Kloudová, A., Svobodová, B., Anubhav, A., Dubišová, J., Schmidt, M., Kubinová, Š., Jhanwar Uniyal, M., Jendelová, P.: (2017) A green tea polyphenol epigallocatechin-3-gallate enhances neuroregeneration after spinal cord injury by altering levels of inflammatory cytokines. Neuropharmacology. 126: 213-223.
Novotná, B. , Herynek, V., Rössner ml., P., Turnovcová, K., Jendelová, P.: (2017) The effects of grafted mesenchymal stem cells labeled with iron oxide or cobalt-zinc-iron nanoparticles on the biological macromolecules of rat brain tissue extracts. International Journal of Nanomedicine. 12: 4519-4526.
Růžička, J., Machová Urdziková, L., Gillick, J., Amemori, T., Romayuk, N., Kárová, K., Závišková, K., Dubišová, J., Kubinová, Š., Murali, R., Syková, E., Jhanwar-Uniyal, M., Jendelová, P.: (2017) A Comparative Study of Three Different Types of Stem Cells for Treatment of Rat Spinal Cord Injury. Cell Transplantation. 26(4): 585-603.
Růžička, J., Machová Urdziková, L., Svobodová, B. , Amin, A.G., Kárová, K., Dubišová, J., Závišková, K., Kubinová, Š., Schmidt,M., Jhanwar-Uniyal, M., Jendelová, P.: (2017) Combined therapy of Curcumin and Epigallocatechin gallate in an experimental model of spinal cord injury in rats. Neural Regeneration Research. IN PRESS
Syková, E. , Rychmach, P., Drahorádová, I., Konrádová, Š., Růžičková, K., Voříšek, I., Forostyak, S., Homola, A., Bojar, M.: (2017) Transplantation of Mesenchymal Stromal Cells in Patients With Amyotrophic Lateral Sclerosis: Results of Phase I/IIa Clinical Trial. Cell Transplantation. 26(4): 647-658.
Tyzack, G.E., Hall, E.C., Sibley, Ch.R., Cymes, T., Forostyak, S., Carlino, G., Meyer, I.F., Schiavo, G., Zhang, S.Ch., Gibbons, G.M., Newcombe, J., Patani, R., Lakatos, A.: (2017) A neuroprotective astrocyte state is induced by neuronal signal EphB1 but fails in ALS models. Nature Communications. 8: 1164.
Čejka, Č., Čejková, J., Trošan, P., Zajícová, A., Syková, E., Holáň, V.: (2016) Transfer of mesenchymal stem cells and cyclosporine A on alkali-injured rabbit cornea using nanofiber scaffolds strongly reduces corneal neovascularization and scar formation. Histol. Histopath.,969-980.
Čejková, J., Čejka, Č., Trošan, P., Zajícová, A., Syková, E., Holáň, V.: (2016) Treatment of alkali-injured cornea by cyclosporine A-loaded electrospun nanofibers - An alternative mode of therapy. Exp. Eye Res., 147:128-37.
Forostyak, O., Butenko, O., Anděrová, M., Forostyak, S., Syková, E., Verkhratsky, A., Dayanithi, G.: (2016) Specific profiles of ion channels and ionotropic receptors define adipose- and bone marrow derived stromal cells. Stem Cell Res., 16(3): 622-634.
Forostyak, O., Forostyak, S., Kortus, Š., Syková, E., Verkhratsky, A., Dayanithi, G.: (2016) Physiology of Ca(2+) signalling in stem cells of different origins and differentiation stages. Cell Calcium, 59(2-3): 57-66.
Herynek, V., Turnovcová, K., Veverka, P., Dědourková, T., Žvátora, P., Jendelová, P., Gálisová, A., Kosinová, L., Jiráková, K., Syková, E.: (2016) Using ferromagnetic nanoparticles with low Curie temperature for magnetic resonance imaging-guided thermoablation. Int. J. Nanomed., 11: 3801-3811.
Chudičková, M. , Brůža, P., Zajícová, A., Trošan, P., Svobodová, L., Javorková, E., Kubinová, Š., Holáň, V.: (2015) Targeted neural differentiation of murine mesenchymal stem cells by a protocol simulating the inflammatory site of neural injury. J. Tissue Eng. Regen. Med., IN PRESS
Jelínek, M., Bačáková, L., Remsa, J., Kocourek, T., Mikšovský, J., Písařík, P.,Vandrovcová, M., Filová, E.,Kubinová, Š.: (2016) Hybrid Laser Technology for Creation of Doped Biomedical Layers. Journal of Materials Science and Chemical Engineering. 4 (1) 98-104.
Jendelová, P., Kubinová, Š., Sandvig, I., Erceg, S., Sandvig, A., Syková, E.: (2016) Current developments in cell - and biomaterial-based approaches for stroke repair. Expert Opin Biol Ther., 16(1): 43-56.
Jiráková, K., Šeneklová, M ., Jirak, D., Turnovcová, K., Vosmanská, M., Babič, M., Horák, D., Veverka, P., Jendelová, P.: (2016) The effect of magnetic nanoparticles on neuronal differentiation of iPS-derived neural precursors Int J Nanomedicine, 6: 6267-6281.
Kaman, O., Dědourková, T., Koktan, J., Kuličková, J., Maryško, M., Veverka, P., Havelek, R., Královec, K., Turnovcová, K., Jendelová, P., Schröfel, A., Svoboda, L.: (2016) Silica-coated manganite and Mn-based ferrite nanoparticles: a comparative study focused on cytotoxicity. J. Nanopart. Res., 18 (4): 100.
Kortus, Š., Srinivasan, C., Forostyak, O., Ueta, Y., Syková, E., Chvátal, A., Zápotocký, M., Verkhratsky, A., Dayanithi, G.: (2016) Physiology of spontaneous [Ca2+]i oscillations in the isolated vasopressin and oxytocin neurones of the rat supraoptic nucleus. Cell Calcium., 59(6): 280-288.
Kortus, Š., Srinivasan, C., Forostyak, O., Zápotocký, M., Ueta, Y., Syková, E., Chvátal, A., Verkhratsky, A., Dayanithi, G.: (2016) Sodium-calcium exchanger and R-type Ca2+ channels mediate spontaneous [Ca2+]i oscillations in magnocellular neurones of the rat supraoptic nucleus. Cell Calcium., 59(6): 289-298.
Lukovic, D., Diez Lloret, A., Stojkovic, P., Rodríguez-Martínez, D., Perez Arago, M.A., Rodriguez-Jimenez F.J., González-Rodríguez, P., López-Barneo, J., Syková, E., Jendelová, P., Kostic, J., Moreno-Manzano, V., Stojkovic,M., Shomi S Bhattacharya, S.S, Erceg S.: (2016) Highly efficient neural conversion of human pluripotent stem cells in adherent and animal-free conditions. Stem Cells Transl. Med., IN PRESS
Lukovic, D., Moreno-Manzano, V., Rodriguez-Jimenez, F.J., Vilches, A., Syková,E., Jendelová, P.,Stojkovic, M., Erceg S.: (2016) hiPSC Disease Modeling of Rare Hereditary Cerebellar Ataxias: Opportunities and Future Challenge. Neuroscientist ,IN PRESS
Lunov, O., Zablotskii, V., Churpita, O., Jaeger, A., Polívka, L ., Syková, E., Terebová, N., Kulikov, A., Kubinová, Š., Dejneka, A.: (2016) Towards the understanding of non-thermal air plasma action: effects on bacteria and fibroblasts. RSC Adv., 6(30) 25286-25292.
Lunov, O., Zablotskii, V., Churpita, O., Jäger, A., Polívka, L., Syková, E., Dejneka, A., Kubinová, Š.: (2016) The interplay between biological and physical scenarios of bacterial death induced by non-thermal plasma. Biomaterials., 82: 71-83.
Lunova, M., Zablotskii, V., Dempsey, N.M., Devillers, T., Jirsa, M., Syková, E., Kubinová, Š., Lunov, O., Dejneka, A.: (2016) Modulation of collective cell behaviour by geometrical constraints. Integr. Biol., 8(11): 1099-1110.
Macková, H., Plichta, Z., Proks, V., Kotelnikov, I., Kučka, J., Hlídková, H., Horák, D., Kubinová, Š, Jiráková, K.: (2016) RGDS- and SIKVAVS-Modified Superporous Poly(2-hydroxyethyl methacrylate) Scaffolds for Tissue Engineering Applications. Macromol. Biosci., IN PRESS.
Machová Urdzíková, L., Kárová, K., Růžička, J., Kloudová, A., Shannon, C., Dubišová, J., Murali, R., Kubinová, Š., Syková, E., Jhanwar-Uniyal, M., Jendelová, P.: (2016) The Anti-Inflammatory Compound Curcumin Enhances Locomotor and Sensory Recovery after Spinal Cord Injury in Rats by Immunomodulation. Int. J. Mol. Sci., 17(1).
Novotná, B., Turnovcová, K., Veverka, P., Rössner, P. Jr., Bagryantsevá, Y., Herynek, V., Zvatora, P., Vosmanská, M., Klementová, M., Syková, E., Jendelová, P.: (2016) The impact of silica encapsulated cobalt zinc ferrite nanoparticles on DNA, lipids and proteins of rat bone marrow mesenchymal stem cells. Nanotoxicology, 10(6): 662-670.
Růžička, J., Kulijewicz-Nawrot, M., Rodrigez-Arellano, J.J., Jendelová,P., Syková, E.: (2016) Mesenchymal Stem Cells Preserve Working Memory in the 3xTg-AD Mouse Model of Alzheimer's Disease. Int. J. Mol. Sci., 17(2): 152.
Růžička, J., Machová Urdziková, L ., Gillick, J., Amemori, T., Romayuk, N., Kárová, K., Závišková, K., Dubišová, J., Kubinová, Š., Murali, R., Syková, E., Jhanwar-Uniyal, M., Jendelová, P.: (2016) A comparative study of three different types of stem cells for treatment of rat spinal cord injury. Cell Transplant., IN PRESS
Syková, E ., Rychmach, P., Drahorádová, I., Konrádová, Š., Růžičková, K., Voříšek, I., Forostyak, S., Homola, A., Bojar, M.: (2016) Transplantation of mesenchymal stromal cells in patients with amyotrophic lateral sclerosis: Results of Phase I/IIa clinical trial. Cell Transplant., IN PRESS
Školoudik, L., Chrobok, V., Kalfert, D., Koči, Z., Syková, E., Chumak, T., Popelář, J., Syka. J., Laco, J., Dědková, J., Dayanithi, G., Filip, S.: (2016) Human multipotent mesenchymal stromal cells in the treatment of postoperative temporal bone defect: an animal model. Cell Transplant., 25(7): 1405-1414.
Šponer, P., Filip, S., Kučera, T., Brtková, J., Urban,K., Palička, V., Kočí, Z., Syka, M., Bezrouk, A., Syková, E.: (2016) Utilizing Autologous Multipotent Mesenchymal Stromal Cells and -Tricalcium Phosphate Scaffold in Human Bone Defects: A Prospective, Controlled Feasibility Trial. Biomed Res. Int., 2076061.
Tukmachev, D., Forostyak, S., Kočí, Z., Závišková, K., Vacková, I., Výborný, K., Sandvig, I., Sandvig, A., Medberry, C.J., Badylak, S.F., Syková, E., Kubinová, Š.: (2016) Injectable Extracellular Matrix Hydrogels as Scaffolds for Spinal Cord Injury Repair. Tissue Eng., 22(3-4): 306-317.
Voříšek, I., Syka, M., Vargová, L.: (2016) Brain Diffusivity and Structural Changes in the R6/2 Mouse Model of Huntington Disease. J. Neurosci. Res., IN PRESS.
Zablotskii, V., Lunov, O., Kubinová, Š., Polyaková, T., Syková, E., Dejneka, A.: (2016) Effects of high-gradient magnetic fields on living cell machinery. J. Phys. D-Appl. Phys., 49: 493003.
Nové terapeutické přístupy neuronální regenerace po poranění míchy pomocí funkcionalizovaných mikrostrukturovaných hydrogelů a kmenových buněk, GA ČR 17-11140S, Spoluřešitel Pavla Jendelová, 2017–2019
Léčba glioblastomu pomocí superparamagnetických nanočástic na bázi oxidů železa s povrchově konjugovaným léčivem GA ČR 17-04918S, Řešitel Pavla Jendelová, 2017–2019
Experimentální transplantace buněk retinálního pigmentového epitelu na modelu velkého zvířete, GAČR 18-04393S, spoluřešitel Mgr. Slaven Erceg, PhD, 2018-2020
MikroRNA v poranění nervové soustavy: potenciální úloha a terapeutický význam, GAČR 18-21942S hlavní řešitel Mgr. Nataliya Romanyuk, PhD, 2018-2020
Studium signálních drah spojených se sekundární reakcí, tvorbou reaktivních kyslíkových radikálů a zánětu při poranění míchy a následné regeneraci. MŠMT program InterExcelence, podprogram InterAction LTAUSA17120, hl. řešitel Doc. RNDr Pavla Jendelová, PhD, 2017-2020.
Ústav klinické a experimentální medicíny IKEM
Ústav makromolekulární chemie AVČR
Fyzikální ústav AVČR
2. Lékařská fakulta, Univerzita Karlova
Lékařská fakulta Hradec Králové
Fakulta biomedicínského inženýrství, ČVUT
© Copyright 2018. All Rights Reserved. Stránky vytvořila agentura WebMotion.