

Oddělení se zabývá morfologickými a elektrofyziologickými vlastnostmi astrocytů a polydendrocytů (NG2 gliových buněk) v patofyziologii globální a fokální cerebrální ischemie a v progresi Alzheimerovy choroby a mechanismy vápníkové signalizace u gliových buněk.
Mgr. Jana Turečková, Ph.D.
E-mail: jana.tureckova@iem.cas.cz
Tel.: +420 241 062 058
Ing. Miroslava Anděrová, CSc.
RNDr. Martina Chmelová, Ph.D.
Mgr. Jana Turečková, Ph.D.
Doc. MUDr. Lýdia Vargová, Ph.D.
Mgr. Tereza Filipi
Mgr. Zuzana Heřmanová
Mgr. Monika Kamenická
Mgr. Denisa Belov Kirdajová
Mgr. Tomáš Knotek
Mgr. Ján Kriška
Mgr. Petra Suchá
Bc. Daniela Kročianová
Bc. Ondřej Vaňátko
Ing. Markéta Hemerová
Helena Pavlíková
V této práci jsme identifikovali několik dosud neznámých rozdílů mezi profily genové exprese NG2 buněk a oligodendrocytů a charakterizovali specifické geny přispívající ke zrání oligodendrocytů a fenotypickým změnám NG2 buněk po fokální cerebrální ischémii. Navíc naše výsledky naznačují, že na rozdíl od patologie Alzheimerovy choroby získají NG2 buňky po ischemickém poškození multipotentní fenotyp.
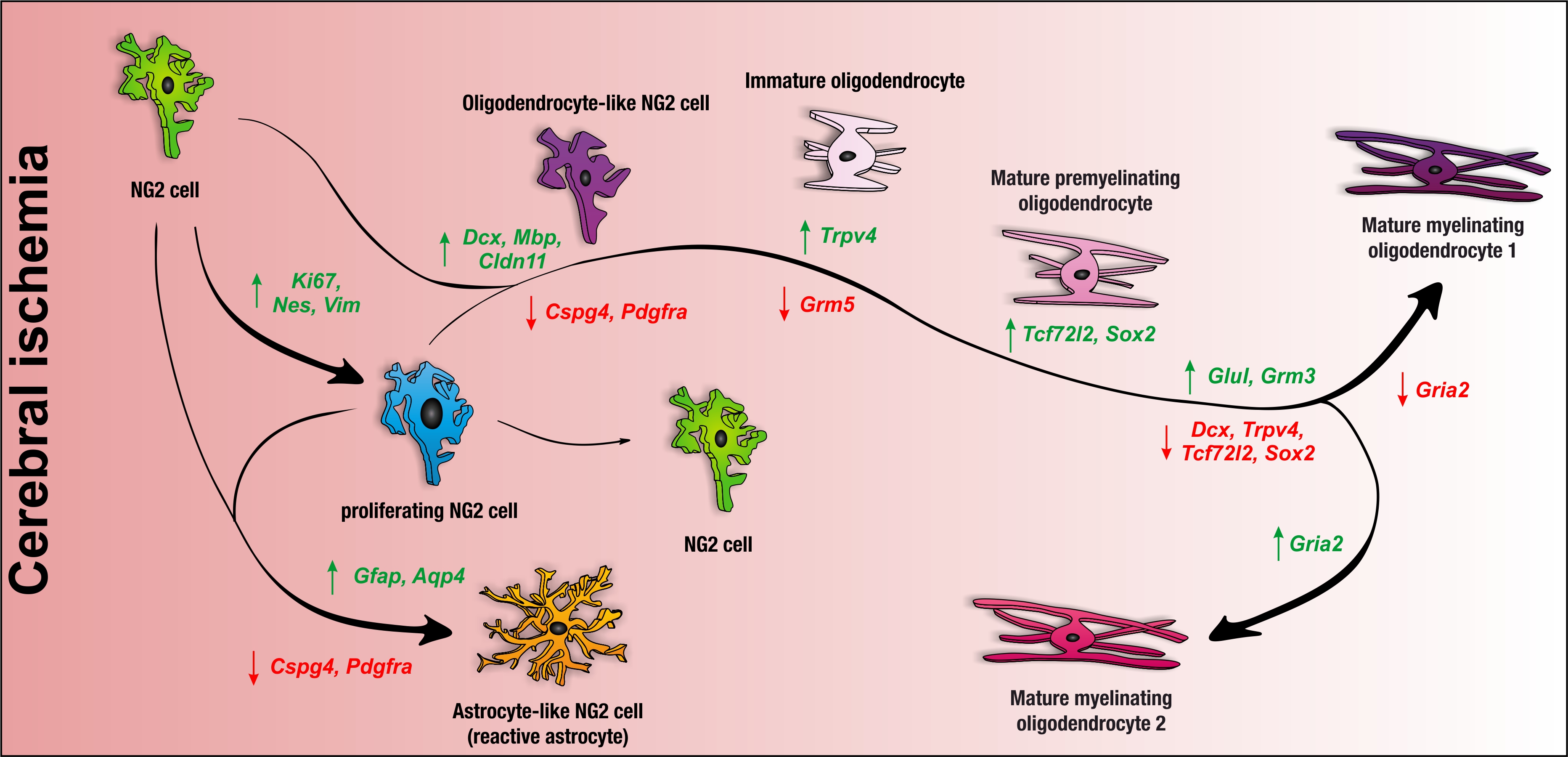
Významné funkce buněk oligodendrogliální linie v post-ischemické regeneraci. Po fokální cerebrální ischémii NG2 buňky získají multipotentní fenotyp; nejprve se podílejí na tvorbě gliální jizvy tím, že diferencují v reaktivní astrocyty, pak dávají vznik i oligodendrocytům - a tak se účastní remyelinizace. Šipky označují upregulaci (zelené šipky) nebo downregulaci (červené šipky) genů.
Spolupráce: Biotechnologický ústav AV ČR, v.v.i.; Ústav neurověd 2. LF UK
Publikace:
Valný, M; Honsa, P; Waloschková, E; Matušková, H; Kriška, J; Kirdajová, D; Androvič, P; Valihrach, L; Kubista, M; Anděrová, M. A single-cell analysis reveals multiple roles of oligodendroglial lineage cells during post-ischemic regeneration. Glia. 2018 May;66(5):1068-1081. doi: 10.1002/glia.23301.
Ochranná schopnost komplexů extracelulární matrix je v thalamu myší s deficitem spojovacího proteinu Bral2 snížená a ovlivňuje tak difuzivitu tkáně u starých, ale ne mladých zvířat. Deficit Bral2, který stabilizuje komplexy extracelulární matrix, vede k redukci perineurálních sítí a axonálních obalů ve ventroposteromediálním jádře thalamu (VPM) u mladých a starých zvířat, ale pokles extracelulárního objemu jsme pozorovali pouze u starých zvířat. Výsledky naznačují, že vliv deficitu Bral2 na difúzi ve VPM je pravděpodoně nepřímý a je způsoben zvýšeným poškozením neuronů s chybějícími ochrannými obaly během stárnutí.
S věkem související změny difuzivity a složení ECM thalamu u Bral2 deficientních myší. Deficit spojovacího proteinu Bral2 je spojen s rozpadem axonálních obalů s obsahem brevikanu (šipka) a významně ovliňuje difuzivitu v thalamickém ventroposteromediálním jádře thalamu u starých, ale ne mladých myší.
Spolupráce: 2LF UK, Praha
Publikace:
Cicanič, M; Edamatsu, M; Bekku, Y; Voříšek, I; Oohashi, T; Vargová, L. A deficiency of the link protein Bral2 affects the size of the extracellular space in the thalamus of aged mice. J Neurosci Res. 2018 Feb;96(2):313-327. doi: 10.1002/jnr.24136.
Ischemická či traumatická poranění centrálního nervového systému (CNS) zvyšují proliferaci NG2 buněk a rozšiřují jejich diferenciační potenciál, což může významně přispět k regeneraci poškozené nervové tkáně. Přehledný článek shrnuje dosavadní poznatky týkající se proliferace a diferenciace NG2 buněk v embryogenezi a v postnatálním CNS za fyziologických i patologických podmínek, s důrazem na úlohu signálních molekul, růstových faktorů, hormonů a dokonce i neurotransmiterů na diferenciační potenciál NG2 buněk. Tyto buňky jsou především významným zdrojem oligodendrocytů, avšak po poranění CNS (demyelinizace, trauma nebo ischemie), proliferace těchto buněk prudce roste a jejich diferenciační potenciál se rozšiřuje.
Proliferace a diferenciace NG2 buněk za fyziologických a patologických podmínek v CNS. Ve vyvíjejícím CNS dávají NG2 buňky vznik astrocytům a oligodendrocytům, avšak v důsledku ischemického či traumatického poškození CNS dávají tyto buňky vznik oligodendrocytů, reaktivním astrocytům a za určitých podmínek i nezralým neuronům.
Publikace:
Valný, M; Honsa, P; Kriška, J; Anděrová, M. Multipotency and therapeutic potential of NG2 cells, Biochemical Pharmacology, 2017, Volume: 141 Pages: 42-55 Special Issue DOI: 10.1016/j.bcp.2017.05.008.
NG2 buňky představují v nepoškozené nervové tkáni především progenitory oligodendrocytů. Za patologických podmínek se uplatňuje jejich široký diferenciační potenciál a mohou se podílet na vzniku reaktivních astrocytů. Tato práce předkládá důkazy, že jedním z faktorů, které zásadně ovlivňují diferenciaci NG2 buněk do reaktivních astrocytů při fokální cerebrální ischemii, je morfogen „sonic hedgehog” (Shh). Výsledky naznačují, že Shh přímo ovlivňuje utváření a složení gliální jizvy, což následně ovlivňuje rozsah ischemického poškození.
Publikace:
Honsa, P; Valný, M; Kriška, J; Matušková, H; Harantová, L; Kirdajová, D; Valihrach, L; Androvič, P; Kubista, M; Anděrová, M. Generation of reactive astrocytes from NG2 cells is regulated by sonic hedgehog. Glia. 2016 Sep;64(9):1518-31. doi: 10.1002/glia.23019.
K objasnění změn difuzivity mozku u Huntingtonovy choroby (HD), jsme porovnali výsledky dvou nezávislých difúzních metod společně s analýzou histologických změn tkáně. Změny v magnetické rezonanci většinou odpovídali změně extracelulárního objemu, spojenému s úbytkem neuronů. Různý stupeň astrogliózy a/nebo exprese extracelulární matrix, které rovněž ovlivňuje difuzivitu mozku, však částečně kompenzuje buněčnou ztrátu a může zapříčinit nekonzistenci výsledků početných HD studií.
Změny difuzivity mozku a struktury tkáně v globus pallidus u myšího modelu Huntigtonovy choroby. Zvětšení extracelulárního objemu a pokles ADCw v globus pallidus jsou výsledkem změn v struktuře tkáně, které mohou protichůdně ovlivňovat difuzivitu mozku: výrazného úbytku neuronů, snížené exprese extracelulární matrix a remodelace astrocytů vlivem astrogliózy.
Publikace:
Voříšek, I; Syka, M; Vargová, L. Brain Diffusivity and Structural Changes in the R6/2 Mouse Model of Huntington Disease. J Neurosci Res. 2016 Oct 11. doi: 10.1002/jnr.23965.
V této práci jsme se zaměřili na expresní profily glutamátových receptorů u gliových buněk v mozkové kůře GFAP/EGFP myší, především na expresi podjednotek NMDA receptoru, jak na genové, tak i proteinové úrovni. Ukázali jsme, že exprese GluN3A podjednotky stoupá v post-ischemických gliích a funkční studie ukázala, že propustnost NMDA receptoru pro vápník v post-ischemických gliích značně snížena.
Focal ischemia increases expression of most of the glutamate receptors (GluRs) in GFAP/EGFP glia. As for the NMDA receptor subunits, immunohistochemical analysis confirmed their presence in GFAP/EGFP glia, and their detection was even increased after ischemic insult. The Ca2+ imaging results indicate diminished NMDA receptor Ca2+ permeability after focal ischemia, which is probabl due to the involvement of GluN3A subunit.
Immunohistochemical analysis of the GluN1, GluN2A-D and GluN3A-B subunits of the NMDA receptors in the cortex of adult GFAP/EGFP mice under control conditions (CTRL) and 14 days after MCAo (D14). Coronal brain sections from CTRL (A) and D14 (B) animals stained with triphenyltetrazolium chloride. The white color in B indicates the volume of ischemic tissue at D14. The boxed areas indicate the regions in which the immunohistochemical analysis was performed. The arrowheads in C - P indicate the overlay of GFAP/EGFP+ cells and NMDA subunit staining – see figure insets for detailed images of cells in white rectangles. Note the overlap of the EGFP signal with GluN3A staining in CTRL tissue and GluN1, GluN2B-D and GluN3A staining at D14. The same scale bar applies to all non-inset images.
Pomocí genového profilování, imunohistochemie a elektrofyziologických metod jsme identifikovali a charakterizovali hyperpolarizací a nukleotidy regulované (HCN) kationtové kanály u reaktivních astrocytů v post-ischemické tkáni. Vzhledem k tomu, že HCN kanály jsou především propustné pro sodné a draselné ionty, mohou významně ovlivňovat regulaci objemu astrocytů a následně, i rozsah poškození nervové tkáně. HCN kanály u astrocytů tak mohou být významným cílovým proteinem v léčbě ischemicky poškozené nervové tkáně.
Exprese Hcn genů je významně zvýšena u astrocytů v mozkové kůře GFAP/EGFP myší po fokální cerebrální ischemii - RT-qPCR profilování na úrovni jednotlivých buněk. (A)Schéma ukazuje oblasti mozku, z které byly EGFP+ buňky izolovány. Ischemické poškození mozku bylo vizualizováno pomocí barvení tetrazolium chloridem. (B) Procenta EGFP+ buněk v post-ischemické mozkové kůře myši (7 a 14 dní po fokální cerebrální ischemii (FCI), D7 a 2W) exprimují Hcn1, 2, 3 a 4. (C) Relativní hladiny exprese Hcn1-4 genů u EGFP+ buněk v nepoškozené (kontrola) a ischemicky poškozené mozkové kůře; významný nárůst exprese těchto genů byl detekován 2W po FCI.
Imunohistochemická analýza exprese HCN1 kanálů v CA1 oblasti nepoškozeného hipokampu a hipokampu 5 týdnů po globální cerebrální ischemii. Tkáňové řezy byly barveny protilátkou anti-HCN1 a anti-GFAP (gliální fibrilární acidický protein). Šipky ukazují HCN1-pozitivní astrocyty po ischemii (s.p., stratum pyramidale; s.r., stratum radiatum). Měřítko, 50 µm.
Spolupráce: Biotechnologický ústav AV ČR – Prof. Mikael Kubista
Publikace:
Honsa, P; Pivoňková, H; Harantová, L; Butenko, O; Kriška, J; Džamba, D; Rusnaková, V; Valihrach, L; Kubista, M; Anděrová, M. Increased expression of hyperpolarization-activated cyclic nucleotide-gated (HCN) channels in reactive astrocytes following ischemia. Glia 62 (12), 2004–2021. IF 5,466
Ukázali jsme, že delece α-syntrofinu, který je zodpovědný za ukotvení aquaporínu-4 v astrocytární membráně, významně ovlivňuje zvětšování/regulaci buněčného objemu u astrocytů v mozkové kůře v průběhu patologických stavů (in situ). Kvantifikace objemových změn astrocytů ukázala, že delece α-syntrofinu má za následek menší/pomalejší změny objemu astrocytů za podmínek hypoosmotického stresu, deprivace kyslíkem a glukózou a vysokých extracelulárních hladin K+.
Změny objemu v těle a výběžcích u astrocytů za hypotonického stresu, zvýšené mimobuněčné koncentrace K+ a deprivace kyslíkem a glukózou (OGD).
Příspěvek výběžků a buněčného těla k celkovému zvětšování objemu je změněný u astrocytů, kterým chybí α-syntrophin.
Spolupráce: 2LF UK, Praha, Biotechnologický ústav AV ČR
Publikace:
Anděrová, M; Benešová, J; Mikešová, M; Džamba, D; Honsa, P; Kriška, J; Butenko, O; Novosadová, V; Valihrach, L; Kubista, M; Dmytrenko, L; Cicanič, M; Vargová, L. Altered Astrocytic Swelling in the Cortex of α-Syntrophin-Negative GFAP/EGFP Mice, PLoS One. 9(11):e113444. IF 3.534
S použitím metody terčíkového zámku, jsme ukázali, že u astrocytů izolovaných z mozku potkana zvýšené koncentrace intracelulárního sodíku, které jsou detekovány v průběhu ischemie, snižují tok iontů skrze objemově regulované aniontové kanály (VRAC). VRAC jsou aktivovány objemovými změnami astrocytů, atˇ již ischemickým poškozením mozku či hypotonickým stresem. Tato práce je prvním důkazem, že intracelulární koncentrace Na mohou modulovat toky iontů přes membránu astrocytů, jež jsou spjaty s regulací objemu a tedy i s rozvojem mozkového edému v průběhu ischemie.
Zvýšená vnitrobuněčná koncentrace Na+ u kultivovaných potkaních astrocytů snižuje aktivitu VRAC kanálů, která byla měřena pomocí metody terčíkového zámku.
Spolupráce: University of Bologna, Italy, Prof. Stefano Ferroni
Publikace:
Minieri, L; Pivoňková, H; Harantová, L; Anděrová, M; Ferroni, S. Intracellular Na+ inhibits volume regulated anion channel in rat cortical astrocytes, J Neurochemistry, doi: 10.1111/jnc.12962., IF 3.973
Transgenní potkani tgHD51 CAG představují model Huntingtono-vy choroby, který vykazuje charakteristiky shodné s histopatolo-gickými změnami u pacientů trpících formou HD s pozdním nástupem. U tgHD51 CAG potkani jsme sledovali neurodegenerativní procesy (NDP) ve striatu a porovnali je se vzorky mozkové tkáně HD pacientů (post-mortem). Naše analýzy ukázaly, že neurodegenerativní procesy u transgenních potkanů tgHD51 CAG jsou pomalejší a reaktivní glióza není tak rozsáhlá jako u progrese HD u lidí.
Spolupráce: LF UK Hradec Králové
Publikace:
Mazurová, Y; Anděrová, M; Němečková, I; Bezrouk, A. Transgenic Huntington’s disease rat model – what can we learn about the neurodegenerative process? Biomed Res Int. 2014;2014:291531. doi: 10.1155/2014/291531.; (formerly Journal of Biomedicine and Biotechnology); doi:10.1155/2014/291531 IF 2.71
Dach1 gen je v myši exprimován neurálními kmenovými buňkami během rané neurogeneze a jeho exprese pokračuje také v části buněk, které se nalézají v dorsální části postranních komor v dospělém mozku. V této studii jsme ukázali, že buňky, které exprimují Dach1 gen, hrají za fyziologických podmínek roli především v gliogenezi, zatímco po ischemickém poškození tyto buňky vykazují neurogenní diferenciační potenciál, avšak nejsou schopné migrovat do ischemické oblasti, kde by připívaly k regeneraci.
Ischémie zvýšila procento DCX+/GFP+ buněk v dorsální části postranních komor. (A) Graf ukazující procento DCX+ buněk ze všech GFP+ buněk v dorsální části postranních komor. Hvězdičky ukazují významné rozdíly mezi kontrolou a post-ischemickou dorzální částí postranních komor. (B) Obrázek ukazuje DCX+ a GFP+ buňky v dorsální části postranních komor v kontrolním mozku. (C) Obrázek ukazuje DCX+ a GFP+ buněk v dorsální části postranních komor na ipsilaterální straně ischemického mozku. (D) Obrázek ukazuje DCX+ a GFP+ buňky v dorsální části postranních komor na kontralaterální straně ischemického mozku. Všimněte si výrazně zvýšeného počtu GFP+ buněk v dorsální části postranních komor a většího výskytu DCX+ buněk po celé kontralaterální postranní komoře. Šipky ukazují GFP+/DCX+ buňky. Měřítko, 50 µm.
Publikace:
Honsa, P; Pivoňková, H; Anděrová, M. Focal cerebral ischemia induces the neurogenic potential of mouse Dach1-expressing cells in the dorsal part of the lateral ventricles, Neuroscience 240 (2013)39–53, IF 3,38
Astrocyty vykonávají kontrolní a regulační funkce v centrálním nervovém systému a jejich heterogenita je stále předmětem sporu. Pro objasnění této heterogenity během postnatálního vývoje a po lokální mozkové ischemii jsme použili metodu genového profilování na úrovni jedné buňky. Identifikovali jsme 3 populace astrocytů během postnatálního vývoje a další tři subpopulace byly identifikovány během 14 dnů po ischemii: klidové glie, rané reaktivní glie a permanentně reaktivní glie.
Změna v genové expresi EGFP+ buněk po MCAO. (A) Změny v genové expresi velmi exprimovaných astrocytálních/NG2 gliálních markerů a membránových proteinů P50 (modrá) , D3 (oranžová) , D7 (zelená) a D14 (červená). (B) PCA třídění buněk ze všech post- ischemické fázích a P50. Stádia jsou označena barevně ( P50 modrá , D3 oranžová , zelená D7 , D14 červené), a tři skupiny identifikované SOM analýzou jsou označeny symboly (čtverečky pro B3 , kruhy pro B1 a trojúhelníky pro B2. (C) Výskyt buněk ze tří subpopulací v post- ischemické fázích a P50 . Geny pod tabulkou ukazují vysoce exprimované geny v jednotlivých podskupiách. (D)Distribuce buněk v jednotlivých subpopulacích.
Publikace:
Rusňáková, V; Honsa, P; Džamba, D; Stahlberg, A; Kubista, M; Anděrová, M. Heterogeneity of astrocytes: from development to injury - single cell gene expression, PLoS One 2013 Aug 5;8(8), IF 3,703
Objevy posledních 25 let prokázaly aktivní úlohu NMDA receptorů v gliových buňkách. Nicméně, existuje mnoho nevyřešených otázek spojených s NMDA receptory u glií. Hlavním cílem této práce je objasnění těchto nejasností shrnutím výsledků ze všech významných publikací týkajících se astrocytů, oligodendrocytů a polydendrocytů u pokusných zvířat, které jsou dále rozšířené studiemi na lidských gliových buňkách.
Nejpravděpodobnější složení NMDA receptorů v astrocytech, oligodendrocytech a polydendrocytech v jednotlivých oblastech CNS za fyziologických a patologických podmínek. Otazníky označují neznámé složení NMDA receptoru.
Publikace:
Džamba, D; Honsa, P; Anděrová, M. NMDA Receptors in Glial Cells: Pending Questions, Curr Neuropharmacol. 2013 May;11(3):250-62, IF 2,847
Narušení interneuronů a glie jako společný patofyziologický mechanismus u heuristických animálních modelů schizofrenie různého původu
GAČR, P303/19-03016S, 2019 - 2021
Gliové buňky- klíčoví hráči v progresi amyotrofické laterální sklerózy
GAČR, P303/19-02046S, 2019 - 2021
Úloha kanonické Wnt signální dráhy v proliferaci a diferenciaci polydendrocytů po ischemickém poranění nervové tkáně
GAUK, 330119, 2019 - 2021
Úloha gliálních TRPV4 kanálů ve vzniku mozkového edému a post-ischemické regeneraci
GAČR, 20-05770S, 2020 - 2022
Role horizontálního transferu mitochondrií v tvorbě nádorů mozku
GAČR, 20-05942S, 2020 - 2022
Role pohlaví při nástupu ALS u myšího modelu SOD1
GAUK, 158320, 2020 - 2022
Androvic, P., Kirdajova, D., Tureckova, J., Zucha, D., Rohlova, E., Abaffy, P., Kriska, J., Valny, M., Anderova, M., Kubista, M., Valihrach, L.: (2020) Decoding the Transcriptional Response to Ischemic Stroke in Young and Aged Mouse Brain. Cell Rep. 2020 Jun 16;31(11):107777.doi: 10.1016/j.celrep.2020.107777.
Belov Kirdajova, D. , Kriska, J., Tureckova, J., Anderova, M.: (2020) Ischemia-Triggered Glutamate Excitotoxicity From the Perspective of Glial Cells. Front Cell Neurosci. 2020 Mar 19;14:51. doi: 10.3389/fncel.2020.00051. eCollection 2020.
Filipi, T. , Hermanova, Z., Tureckova, J., Vanatko, O., Anderova, M.: (2020) Glial Cells-The Strategic Targets in Amyotrophic Lateral Sclerosis Treatment. J Clin Med. 2020 Jan 18;9(1). pii: E261. doi: 10.3390/jcm9010261.
Kirdajova, D. , Anderova, M.: (2019) NG2 cells and their neurogenic potential. Curr Opin Pharmacol. 2019 Dec 23;50:53-60. doi: 10.1016/j.coph.2019.11.005. [Epub ahead of print]
Kolenicova, D. , Tureckova, J., Pukajova, B., Harantova ,L., Kriska, J., Kirdajova, D., Vorisek, I., Kamenicka, M., Valihrach, L., Androvic, P., Kubista, M., Vargova, L., Anderova, M.: (2019) High potassium exposure reveals the altered ability of astrocytes to regulate their volume in the aged hippocampus of GFAP/EGFP mice. Neurobiol Aging. 2019 Oct 22. pii: S0197-4580(19)30372-0. doi: 10.1016/j.neurobiolaging.2019.10.009. [Epub ahead of print]
Dvorakova, M., Macova, I., Bohuslavova, R., Anderova, M., Fritzsch, B., Pavlinkova, G.: (2019) Early ear neuronal development, but not olfactory or lens development, can proceed without SOX2. Dev Biol. 2020 Jan 1;457(1):43-56. doi: 10.1016/j.ydbio.2019.09.003. Epub 2019 Sep 14.
Chmelová, M. , Suchá, P., Bochin, M., Voříšek, I., Pivoňková, H., Heřmanová, Z., Anděrová, M., Vargová, L.: (2019) The role of aquaporin-4 and transient receptor potential vaniloid isoform 4 channels in the development of cytotoxic edema and associated extracellular diffusion parameter changes. Eur J Neurosci. 2019 Jan 11. doi: 10.1111/ejn.14338.
Pivoňková, H. , Heřmanová, Z., Kirdajová, D., Awadová, T., Malínský, J., Valihrach, L., Žucha, D., Kubista, M., Gálisová, A., Jirák, D., Anděrová, M.: (2018) The Contribution of TRPV4 Channels to Astrocyte Volume Regulation and Brain Edema Formation. Neuroscience. 2018 Dec 1;394:127-143. doi: 10.1016/j.neuroscience.2018.10.028. Epub 2018 Oct 24.
Awadová, T., Pivoňková, H., Heřmanová, Z., Kirdajová, D., Anděrová, M., Malínský, J.: (2018) Cell volume changes as revealed by fluorescence microscopy: Global vs local approaches. J Neurosci Methods. 2018 Aug 1;306:38-44. doi: 10.1016/j.jneumeth.2018.05.026. Epub 2018 Jun 7.
Cicanič, M., Edamatsu, M., Bekku, Y., Voříšek, I., Oohashi, T., Vargová, L.: (2018) A deficiency of the link protein Bral2 affects the size of the extracellular space in the thalamus of aged mice. J Neurosci Res. 96(2):313-327.
Valný, M., Honsa, P., Waloschková, E., Matušková, H., Kriška, J., Kirdajová, D., Androvič, P., Valihrach, L., Kubista, M., Anděrová, M.: (2018) A single-cell analysis reveals multiple roles of oligodendroglial2 lineage cells during post-ischemic regeneration. Glia. 2018 May;66(5):1068-1081. doi: 10.1002/glia.23301. Epub 2018 Feb 2.
Pivoňková H., Anděrová M.: (2017) Altered Homeostatic Functions in Reactive Astrocytes and Their Potential as a Therapeutic Target After Brain Ischemic Injury. Curr Pharm Des. 23(33):5056-5074.
Syková, E., Rychmach, P., Drahorádová, I., Konrádová, Š., Růžičková, K., Voříšek, I., Forostyak, S., Homola, A., Bojar, M.: (2017) Transplantation of Mesenchymal Stromal Cells in Patients With Amyotrophic Lateral Sclerosis: Results of Phase I/IIa Clinical Trial. Cell Transplantation. 26(4): 647-658.
Valný M., Honsa P., Kriška J., Anděrová M.: (2017) Multipotency and therapeutic potential of NG2 cells. Biochem Pharmacol. 141:42-55.
Voříšek, I., Syka, M., Vargová, L.: (2017) Brain Diffusivity and Structural Changes in the R6/2 Mouse Model of Huntington Disease. Journal of Neuroscience Research. 95(7): 1474-1484.
Džamba D., Harantová L., Butenko O., Anděrová, M.: (2015) Glial cells – the key elements of Alzheimer´s disease. Curr. Alzheimer Res., 13(8): 894-911.
Džamba, D., Valihrach, L., Kubista, M., Anděrová, M.: (2016) The correlation between expression profiles measured in single cells and in traditional bulk samples. Scientific Reports, 16(6): 37022.
Forostyak, O., Butenko, O., Anděrová, M., Forostyak, S., Syková, E., Verkhratsky, A., Dayanithi, G.: (2016) Specific profiles of ion channels and ionotropic receptors define adipose- and bone marrow derived stromal cells. Stem Cell Res., 16(3):622-634.
Honsa, P., Valný, M., Kriška, J., Matušková, H., Harantová, L., Kirdajová, D., Valihrach, L., Androvič, P., Kubista, M., Anděrová, M.: (2016) Generation of reactive astrocytes from NG2 cells is regulated by sonic hedgehog. Glia, 64(9): 1518-1531.
Janečková, L., Fafílek, B., Krausová, M., Horázná, M., Vojtěchová, M., Alberich-Jorda, M., Sloncová, E., Galušková, K., Sedláček, R., Anděrová, M., Kořínek, V.: (2016) Wnt Signaling Inhibition Deprives Small Intestinal Stem Cells of Clonogenic Capacity. Genesis, 54(3): 101-114.
Kriška, J., Honsa, P., Džamba, D., Butenko, O., Koleničová, D., Janečková, L., Nahacká, Z., Anděra, L., Kozmík, Z., Taketo, M.M., Kořínek, V., Anděrová, M.: (2016) Manipulating Wnt signaling at different subcellular levels affects the fate of neonatal neural stem/progenitor cells. Brain Res., 1651: 73-87.
Lee, C.Y., Dallérac, G., Ezan, P., Anděrová, M., Rouach, N.: (2016) Glucose Tightly Controls Morphological and Functional Properties of Astrocytes. Front. Aging Neurosci., 8(82): 1-12.
Valný, M., Honsa, P., Kirdajová, D., Kameník, Z., Anděrová, M.: (2016) Tamoxifen in the Mouse Brain: Implications for Fate-Mapping Studies Using the Tamoxifen-Inducible Cre-loxP System. Front. Cell. Neurosci., 10: 243.
Džamba, D., Honsa, P., Valný, M., Kriška, J., Valihrach, L., Novosadová, V., Kubista, M., Anděrová, M.: (2015) Quantitative Analysis of Glutamate Receptors in Glial Cells from the Cortex of GFAP/EGFP Mice Following Ischemic Injury: Focus on NMDA Receptors. Cell Mol Neurobiol. 35(8): 1187-1202.
Džamba D., Harantová L., Butenko O., Anděrová, M.: (2015) Glial cells – the key elements of Alzheimer´s disease. Current Alzheimer Research IN PRESS
Chvátal, A.: (2015) Discovering the structure of nrve tissue: part 1: from Marcello Malpighi to Christian Berres. J. Hist. Neurosci., 24(3): 268-291.
Chvátal, A.: (2015) Jiří Procháska (1749-1820): Part 2: "De structura nervorum"--studies on a structure of the nervous system. J. Hist. Neurosci., 24(1): 1-25.
Chvátal, A.: (2015) Jan Křtitel Boháč (1724-1768) a jeho disertace o bolesti z roku 1746. (Jan Křtitel Boháč (1724-1768) and dissertation on pain from 1746). Bolest, 18(1): 8-20.
Chvátal, A.: (2015) Výzkum struktury nervové tkáně III: od Jana Evangelisty Purkyně (1787–1869) k Ludwigovi Mauthnerovi (1840–1894). Československá fyziologie, 2: 52-72.
Minieri, L., Pivoňková, H., Harantová, L., Anděrová, M., Ferroni S.: (2014) Intracellular Na+ inhibits volume regulated anion channel in rat cortical astrocytes. J. Neurochem. 132(3): 286-300.
Anděrová, M., Benešová, J., Mikešová, M., Džamba, D., Honsa, P., Kriška, J., Butenko, O., Novosadová, V., Valihrach, L., Kubista, M., Dmytrenko, L., Cicanič, M., Vargová, L.: (2014) Altered astrocytic swelling in the cortex of α-syntrophin-negative GFAP/EGFP mice. PloS One. 9(11): e113444.
Honsa, P., Pivoňková, H., Harantová, L., Butenko, O., Kriška, J., Džamba, D., Rusňáková, V., Valihrach, L., Kubista, M., Anděrová, M.: (2014) Increased expression of hyperpolarization-activated cyclic nucleotide-gated (HCN) channels in reactive astrocytes following ischemia. Glia. 62(12): 2004-2021
Chvátal, A.: (2014) Jiří Procháska (1749-1820): Part 1: A Significant Czech Anatomist, Physiologist and Neuroscientist of the Eighteenth Century. J. Hist. Neurosci. 23(4): 367-376
Chvátal, A.: (2014) Discovering the Structure of Nerve Tissue: Part 1: From Marcello Malpighi to Christian Berres. J. Hist. Neurosci. In press.
Mazurová, Y., Anděrová, M., Němečková, I., Bezrouk, A.: (2014) Transgenic Rat Model of Huntington's Disease: A Histopathological Study and Correlations with Neurodegenerative Process in the Brain of HD Patients. Biomed. Res. Int. 2014: 291531.
Dmytrenko, L., Cicanič, M., Anděrová, M., Voříšek, I., Ottersen, O. P., Syková, E., Vargová, L.: (2013) The Impact of Alpha-Syntrophin Deletion on the Changes in Tissue Structure and Extracellular Diffusion Associated with Cell Swelling under Physiological and Pathological Conditions. PLoS One. 8(7): e68044.
Džamba, D., Honsa, P., Anděrová, M.: (2013) NMDA Receptors in Glial Cells: Pending Questions. Curr. Neuropharmacol. 11: 250-262.
Honsa, P., Pivoňková, H., Anděrová, M.: (2013) Focal cerebral ischemia induces the neurogenic potential of mouse Dach1-expressing cells in the dorsal part of the lateral ventricles. Neuroscience. 240: 39-53.
Minieri, L., Pivoňková, H., Caprini, M., Harantová, L., Anděrová, M., Ferroni, S.: (2013) The inhibitor of volume regulated anion channels DCPIB activates TREK potassium channels in cultured astrocytes. Br. J. Pharmacol. 168(5): 1240-1254.
Rusňáková, V., Honsa, P., Džamba, D., Stählberg, A., Kubista, M., Anděrová, M.: (2013) Heterogeneity of Astrocytes: From Development to Injury – Single Cell Gene Expression. PLoS One 8(8): e69734.
Stählberg, A., Rusňáková, V., Forootan, A., Anděrová, M., Kubista, M.: (2013) RT-qPCR work-flow for single-cell data analysis.Methods. 59(1): 80-88.
© Copyright 2018. All Rights Reserved. Stránky vytvořila agentura WebMotion.