Cílená modulace signálních drah v buňce novým typem agonistů muskarinových receptorů, může vést k vývoji léčiv bez vedlejších účinků. (22.7. 2020)
V současné době více než třetina všech léčiv na trhu cílí na receptory v membránách buněk, které jsou spřaženy s vnitrobuněčnými signálními G‑proteiny (tzv. GPCR). Tento typ membránových receptorů se podílí na řízení široké škály fyziologických procesů, počínaje zpracováním smyslových podnětů, přes regulaci chování a nálady, hormonální a imunitní odpovědi až po řízení autonomních funkcí a buněčné proliferace. Proto tyto receptory obecně představují jeden z nejdůležitějších farmakoterapeutických cílů. Tradiční agonisté GPCR aktivují v buňkách obvykle vícero signálních drah, což může mít za následek řadu vedlejších účinků. Látky vedoucí výlučně k aktivaci jedné signální dráhy představují novou generaci vysoce specifických léčiv s méně vedlejšími účinky. Velké úsilí bylo dosud věnováno výzkumu látek vedoucích buď k aktivaci G‑proteinových drah, nebo k signalizační kaskádě přes β‑arrestiny.
V naší laboratoři se zaměřujeme na studium muskarinových acetylcholinových receptorů, které patří k typickým představitelům GPCR. V naší publikaci představujeme zcela nový typ agonistů těchto receptorů, kteří dokážou specificky modulovat signální dráhy na úrovni spřahování receptoru s jednotlivými podtypy G‑proteinů (Obrázek 1A). Zmíněné látky působí výhradně na signální dráhu přes protein Gi, která vede k inhibici adenylát cyklázy a tím ke snížení hladiny cAMP v buňce (Obrázek 1B). Díky tomu jsou tyto látky funkčně selektivní pro muskarinové receptory M2 a M4, jež představují jeden z farmakologických cílů při léčbě bolesti. Nově objevení agonisté mohou vést k vývoji nových analgetik nezpůsobujících návyk jako opiáty, nebo oslabení imunity jako steroidní analgetika. Tato muskarinová analgetika by nezpůsobovala vedlejší účinky zprostředkované aktivací signální dráhy přes protein Gq, jako je inkontinence, nadměrné slinění a pocení a další.
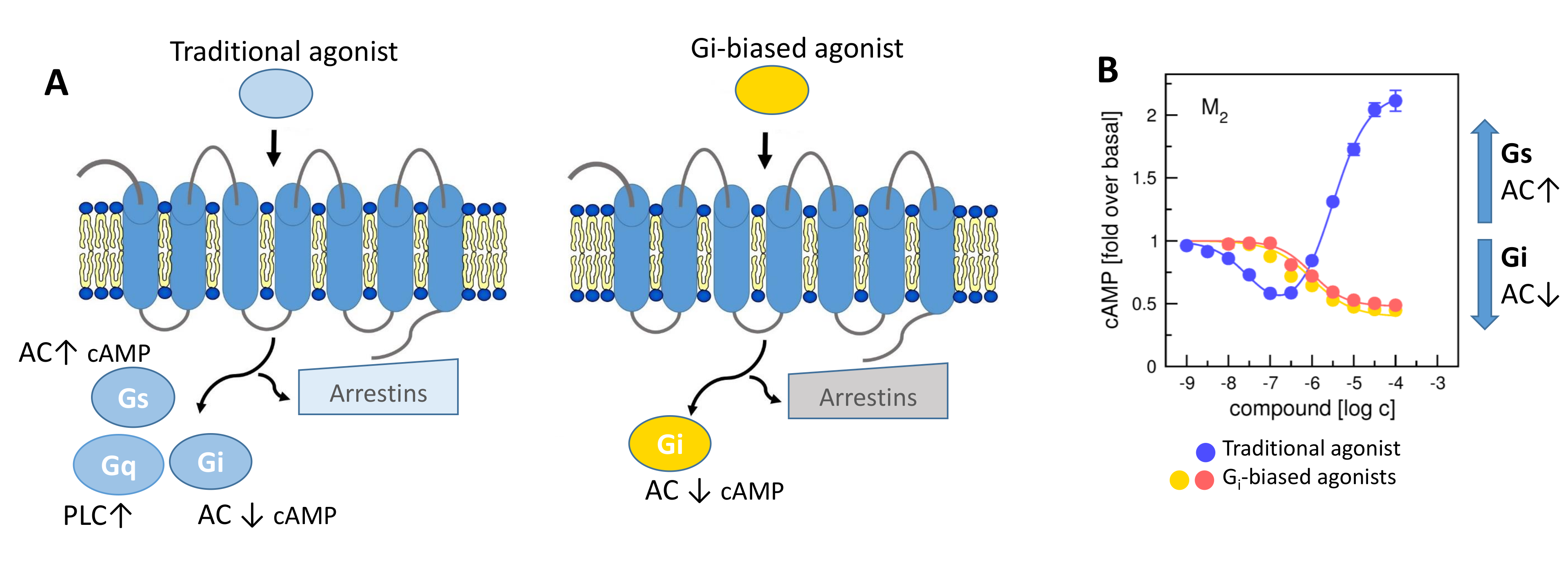
A) Obecné schéma spřahování GPCR s jednotlivými podtypy G-proteinů nebo arrestiny po aktivaci agonistou tradičního typu (vlevo) a agonistou preferujícím aktivaci Gi-proteinu (vpravo). AC, adenylát cykláza; PLC fosfolipáza C. B) Aktivace M2 receptoru tradičním agonistou (modře) stimulujícím Gi i Gs-proteinovou dráhu, což vede ke snížení hladiny cAMP v buňce při nízkých koncentracích agonisty a k nárůstu koncentrace cAMP při vyšších koncentracích agonisty. Aktivace M2 receptoru dvěma různými Gi-preferujícími (Gi-biased) agonisty (červeně, oranžově) stimulujícími pouze Gi-proteinovou dráhu, což vede pouze ke snížení hladiny cAMP.
Randáková A, Nelic D, Ungerová D, Nwokoye P, Su Q, Doležal V, El-Fakahany EE, Boulos J, Jakubík J. Novel M2-Selective, Gi-Biased Agonists of Muscarinic Acetylcholine Receptors. Br J Pharmacol. 2020 May;177(9):2073-2089. doi: 10.1111/bph.14970.
Koncentrace bioaktivního lipidu 5-PAHSA jsou regulovány enzymaticky a připravují tukovou tkáň na syntézu mastných kyselin. (22.7. 2020)
5-PAHSA patří mezi nově objevené lipidy, které jsou příslibem pro léčbu cukrovky a zánětlivých onemocnění, avšak detaily jejich působení nejsou známy. Experimenty na myších a lidských buňkách prokázaly, že 5-PAHSA dokáže podobně jako inzulin dopravit cukr do buněk, avšak poté už funguje odlišně. Zatímco inzulin podněcuje ukládání tuků, 5-PAHSA aktivuje energeticky náročnější metabolickou dráhu, při níž vznikají nové mastné kyseliny. Přijaté cukry se tak využívají metabolicky prospěšněji.
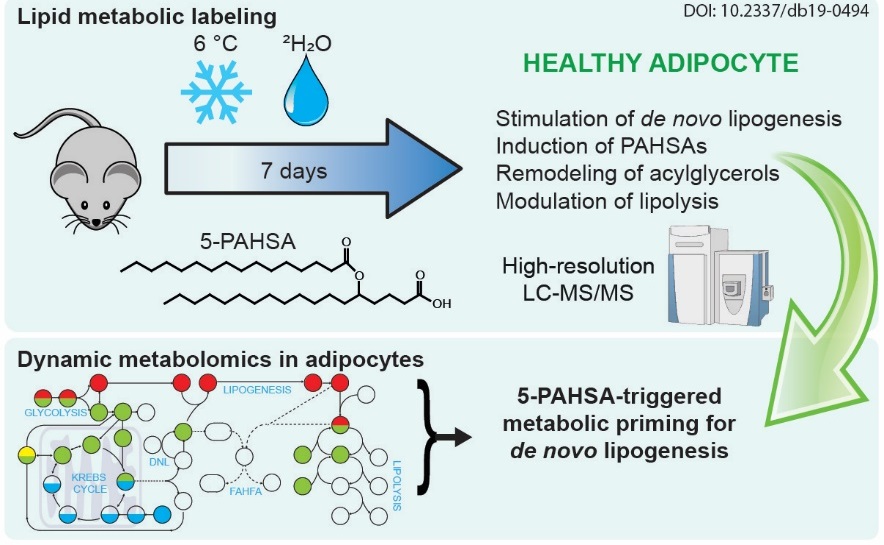
Ovlivnění metabolismu cukrů a lipidů bioaktivním lipidem 5-PAHSA. Pomocí značení metabolických drah a moderních analytických metod na myších modelech byl prokázán pozitivní vliv lipidu 5-PAHSA na zpracování glukózy buňkami.
Lipokine 5-PAHSA is Regulated by Adipose Triglyceride Lipase and Primes Adipocytes for de novo Lipogenesis in Mice. Paluchova V, Oseeva M, Brezinova M, Cajka T, Bardova K, Adamcova K, Zacek P, Brejchova K, Balas L, Chodounska H, Kudova E, Schreiber R, Zechner R, Durand T, Rossmeisl M, Abumrad NA, Kopecky J, Kuda O. Diabetes. 2019 Dec 5. pii: db190494. doi: 10.2337/db19-0494.
Výzkum iontového kanálu TRPA1 může pomoci při objasnění příčin chronické bolesti (3.2. 2020)
Řada závažných onemocnění je doprovázena chronickou bolestí, jejíž molekulární mechanismy nejsou prozatím plně objasněny. Výzkumem iontového kanálu TRPA1, který se uplatňuje v těchto mechanismech, se zabývají vědci z oddělení Buněčné neurofyziologie Fyziologického ústavu AV ČR. Ve spolupráci s laboratoří CBMN Univerzity v Bordeaux prokázali, že aktivita lidského TRPA1 je významně regulována membránovými fosfolipidy na záporných membránových potenciálech. Podařilo se identifikovat vazebné místo TRPA1 kanálu, které interaguje s fosfolipidy při nízkých koncentracích vápenatých iontů. Stejné místo může při vyšších koncentracích vázat regulační protein kalmodulin a modulovat tak iontový kanál způsobem závislým na jeho aktivitě. Tyto nové nálezy naznačují, že pro aktivaci TRPA1 je za fyziologických podmínek důležité správné složení plazmatické membrány zajišťující v oblasti rozhraní mezi podjednotkami převod signálů na otevírání iontového kanálu.
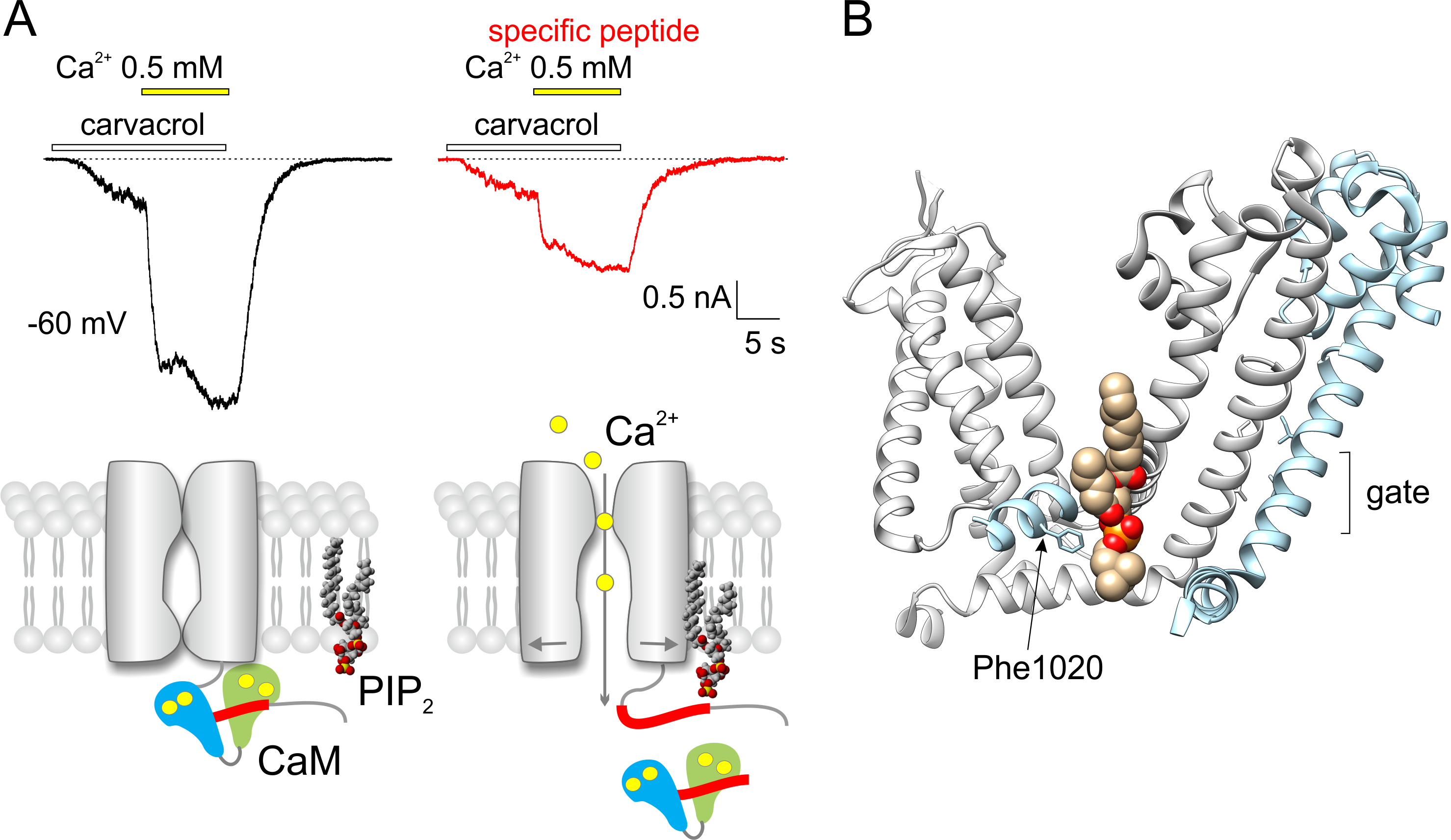
(A) Elektrofyziologické záznamy TRPA1 odpovědí na karvakrol (100 µM) a zvýšenou koncentraci vápenatých iontů (z 0 na 0.5 mM). Záznamy ze dvou F11 buněk snímané pipetou naplněnou (vlevo) kontrolním roztokem a (vpravo) roztokem s přidaným specifickým peptidem T1003-P1034. Dole, navržený mechanizmus, kterým o vazebné místo TRPA1 soutěží kalmodulin (CaM) a fosfolipid (PIP2). (B) Vazebné místo pro fosfolipidy v oblasti rozhraní dvou sousedních podjednotek TRPA1 kanálu. Zobrazena je jen transmembránová část podílející se na vazbě a převodu signalizace do vrátek (gate) kanálu (PDB kód struktury 6pqq). Úloha fenylalaninu Phe1020 v interakci byla prokázána v uvedené studii.
MACIKOVA L, SINICA V, KADKOVA A, VILLETTE S, CIACCAFAVA A, FAHERTY J, LECOMTE S, ALVES ID, VLACHOVA V: Putative interaction site for membrane phospholipids controls activation of TRPA1 channel at physiological membrane potentials. The FEBS Journal 286: 3664-3683, 2019.
Inovativní metoda regulace Forkhead transkripčního faktoru FOXO3 (29.1. 2020)
Studie otištěná v prestižním časopise eLife identifikuje nízkomolekulární sloučeniny, které interagují s transkripčním faktorem Forkhead box O3 (FOXO3) a modulují tak jeho aktivitu.
Protein FOXO3 s charakteristickou DNA-vazebnou doménou je součástí podtřídy O rodiny Forkhead transkripčních faktorů. Tyto transkripční faktory jsou v savčích buňkách klíčovými regulátory buněčné homeostázy, diferenciace, délky života a řízené buněčné smrti. Aktivita FOXO3 také významně přispívá k rezistenci rakovinných buněk vůči chemo- a radioterapii. Nejnovější studie rovněž ukázaly, že se DNA-vazebná doména (DBD) FOXO proteinů účastní protein-proteinových interakcí s dalšími klíčovými regulátory délky života, buněčné smrti a lékové rezistence. Reverzibilní inhibice aktivity FOXO3 prostřednictvím nízkomolekulárních sloučenin by tak mohla podpořit protinádorové imunitní odpovědi.
K inhibici aktivity FOXO3 bylo nejdříve nezbytné identifikovat nízkomolekulární sloučeniny, které by blokovaly interakci mezi FOXO3 DBD a DNA. Na základě struktury FOXO3 DBD a FOXO4 DBD bylo vytvořeno šest různých farmakoforových modelů, které byly využity pro in silico screening databází nízkomolekulárních sloučenin. U vybraných sloučenin byla následně testována schopnost inhibovat funkci FOXO3 jak in vitro, tak i v nádorových buněčných kulturách. Interakce sloučenin s FOXO3 DBD byly charakterizovány pomocí metod NMR spektroskopie a molekulového dokování.
Týmy dr. Veroniky Obšilové z Fyziologického ústavu AV ČR z BIOCEV a prof. Tomáše Obšila z Přírodovědecké fakulty UK ve spolupráci se skupinou prof. M. J. Ausserlechnera z Medical University Innsbruck, Rakousko identifikovaly sloučeniny S9 a její oxalátovou sůl S9OX jako látky schopné inhibovat FOXO3 v nádorových buňkách. Vědci zároveň vyslovili domněnku, že díky svému způsobu vazby na FOXO3 DBD mohou také S9 sloučeniny bránit protein-proteinovým interakcím mezi FOXO3 a jeho vazebnými partnery. Výhodou těchto látek je, že nejsou imunogenní, což umožňuje nastavení dávky a délky aplikace tak, aby byla posílena protinádorová imunita a zároveň byly omezeny nežádoucí efekty inhibice FOXO proteinů u kmenových buněk a somatických tkání. Další výzkum bude zaměřen na zjištění, jestli lze S9 využít jako základ pro vývoj sloučenin schopných specificky modulovat funkce jednotlivých FOXO transkripčních faktorů.
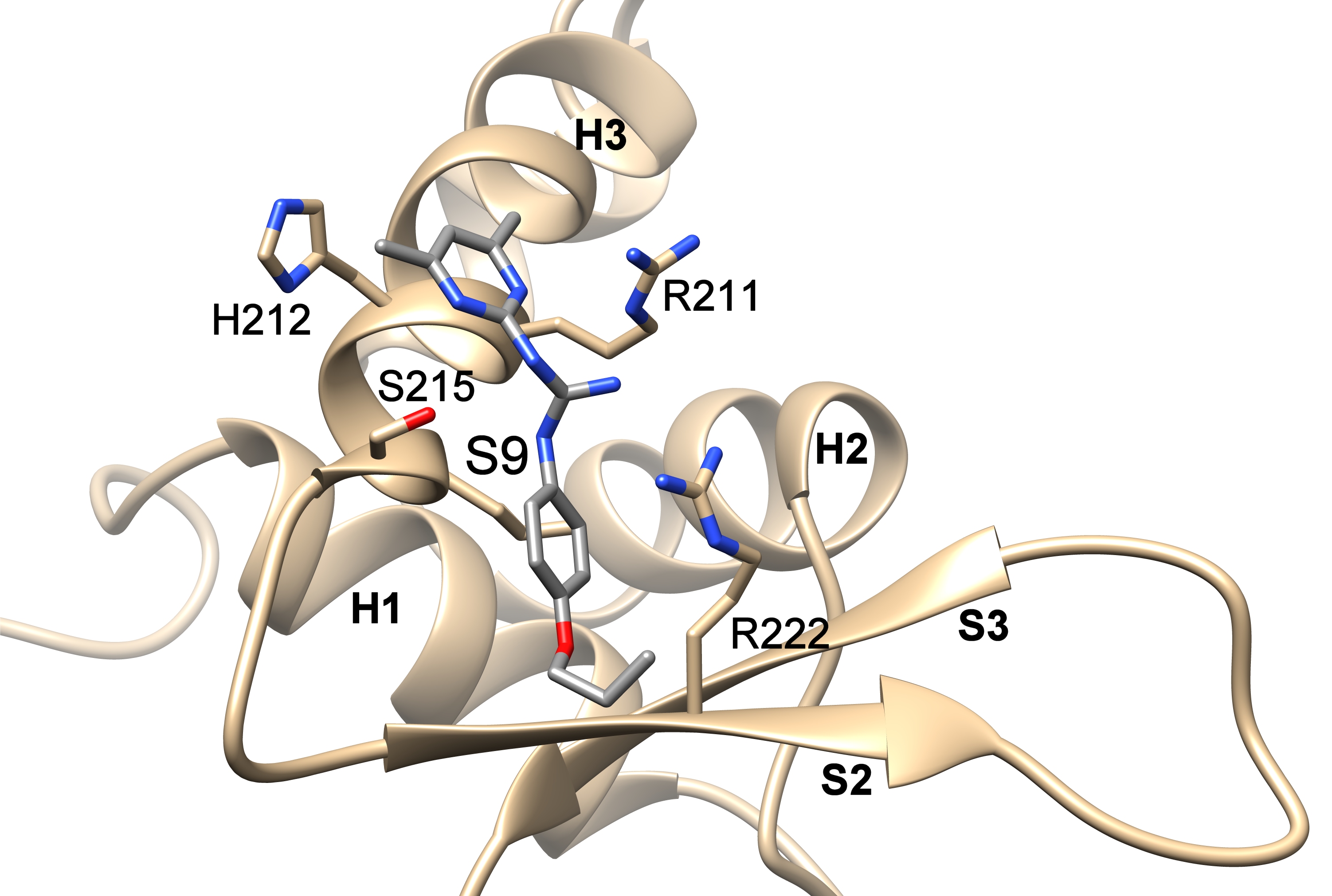
Sloučeniny S9 blokují DNA-vazebný povrch Forkhead transkripčního faktoru FOXO3. Na obrázku je znázorněn strukturní model DNA-vazebné domény FOXO3 s navázanou sloučeninou S9 založený na datech z měření jaderné magnetické resonance a molekulového dokování.
Hagenbuchner, J.+, Obšilová, V.+, Kaserer, T.+, Kaiser, N., Rass, B., Pšenáková, K., Dočekal, V., Alblová, M., Kohoutová, K., Schuster, D., Aneichyk, T., Veselý, J., Obexer, P., Obšil, T.*, Ausserlechner, M. J.* Modulování transkripční aktivity FOXO3 malými DBD-vazebnými molekulami. eLife. 2019, 8(Dec 4), e48876. doi: 10.7554/eLife.48876
Transkripční faktor Hif-1a je nezbytný pro správný vývoj sympatického nervového systému a inervaci srdce (16.1. 2020)
Hypoxií indukovaný faktor 1 (Hif-1) je hlavním regulátorem transkripční odpovědi buněk na sníženou dostupnost kyslíku. Výzkum probíhající v laboratořích Biotechnologického a Fyziologického ústavu AV ČR a 1. Lékařské fakulty UK ukázal, že genetická mutace genu Hif-1a potlačuje embryonální vývoj pregangliových a postgangliových neuronů sympatického nervového systému a negativně ovlivňuje sympatickou inervaci srdce, která hraje primární úlohu při regulaci tepové frekvence a srdeční kontraktility při zátěži. U myši s podmíněnou delecí genu Hif-1a byl zjištěn anomální vývoj architektury koronárního řečiště a snížená kontraktilní funkce srdce. Tyto nové nálezy ukazují, že dysfunkce tohoto transkripčního faktoru může vést k rozvoji závažných kardiovaskulárních onemocnění spojených s poruchou rovnováhy autonomního nervového systému a zároveň otevírají nové možnosti léčby těchto onemocnění v budoucí klinické praxi.
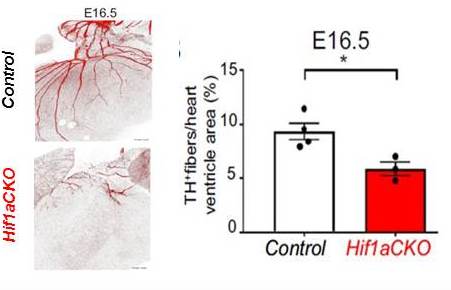
Zhoršený vývoj sympatické inervace srdce s delecí Hif-1a (Hif1aCKO): Immunohistochemická detekce nervových vláken pomocí tyrozin hydroxylázy (TH) a kvantifikace TH-pozitivních vláken u kontrolních and Hif1aCKO srdcí v embryonálním stádiu E16.5.
Bohuslavová, Romana - Čerychová, Radka - Papoušek, František - Olejníčková, Veronika - Bartoš, M. - Goerlach, A. - Kolář, František - Sedmera, David - Semenza, G.L. - Pavlínková, Gabriela: HIF-1 alpha is required for development of the sympathetic nervous system. Proceedings of the National Academy of Sciences of the United States of America. Roč. 116, č. 27 (2019), s. 13414-13423. ISSN 0027-8424, IF: 9.580, 2018.
Načíst další




