

Je především zaměřena na vývoj a přípravu tkáňových náhrad, především biodegradabilních a na bázi nanovláken a pěn, modelování proteinových struktur, ale také vyhledávání možností praktického využití výsledků. Pracoviště vyvíjí technologii uvolňování bioaktivních látek s využitím různých typů nanovlákenných nosičů, syntetických nebo nativních růstových faktorů, což umožňuje řízený přísun živin a léků přímo do místa defektu. Vyvíjejí se umělé chrupavčité a kostní náhrady pro klinické využití v ortopedii, nanovlákenné nosiče pro hojení kožních defektů a incisionální hernie.
Mgr. Michala Rampichová, Ph.D.
E-mail: michala.rampichova@iem.cas.cz
Tel.: +420 241 062 692
Mgr. Eva Filová, Ph.D.
Mgr. Michala Rampichová, Ph.D.
Ing. Lucie Wolfová, Ph.D.
Mgr. Andrea Staffa, Ph.D. (MD)
Mgr. Jana Daňková, Ph.D. (MD)
RNDr. Věra Hedvičáková, Ph.D.
Mgr. Věra Sovková, Ph.D. (MD)
MUDr. et Ing. Karolína Vocetková, Ph.D. (MD)
Mgr. Jana Hlinková, Ph.D.
Mgr. Barbora Voltrová (MD)
Mgr. Veronika Hefka Blahnová
Mgr. Radmila Žižková
Mgr. Eva Šebová
Viktorie Ročková, MSc.
V rámci studie byly na xenogenní kostní štěp SmartBone® navázány biomimetické peptidy P2 a P6. Po nasazení lidských mezenchymálních kmenových buněk z kostní dřeně (MSC) bylo sledováno ovlivnění bioaktivity nosičů. Oba peptidy i jejich kombinace působily na buňky v mnoha ohledech. Fyzikální navázání na štěp s využitím organických rozpouštědel ani sterilizace etylen oxidem nijak nezhoršily biologickou aktivitu peptidů. Především peptid P6 podporoval osteogenní procesy a aktivoval dráhy vedoucí k mineralizaci mezibuněčné hmoty.
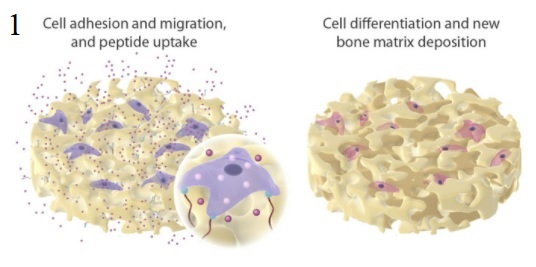 Hybridní kostní štěp SmartBone® s biomimetickými peptidy byl osazen mezenchymálními kmenovými buňkami (MSC), které následně proliferovaly, diferencovaly do osteoblastů a produkovaly mineralizovanou kostní mezibuněčnou hmotu
Hybridní kostní štěp SmartBone® s biomimetickými peptidy byl osazen mezenchymálními kmenovými buňkami (MSC), které následně proliferovaly, diferencovaly do osteoblastů a produkovaly mineralizovanou kostní mezibuněčnou hmotu

Vizualizace hMSC v hybridním kostním štěpu SmartBone® s biomimetickými peptidy P2, P6, směsí P2 a P6 a kontrola (SBN). Buněčný cytoskelet byl obarven phalloidinem (zelené) a jádra pomocí DAPI (modrá) a pozorovány pomocí laserového konfokálního mikroskopu. Měrka: 100 μm.
V rámci studie jsme testovali bioresorbovatelný nosič obsahující anorganický hydroxyapatit, trikalciumfosfát s organickým kolagenem a oxidovanou celulózu obohacený o stabilizovaný fibroblastový růstový faktor-2 (FGF2-STAB®), s funkčním poločasem rozpadu více než 20 dní při 37°C. Biokompatibilita nosiče byla prokázána in vitro pomocí lidských mezenchymálních kmenových buněk (MSC). Nosič byl dále použit pro mezitělovou fúzi bederní páteře na modelu prasete. Kvalita fúze páteře ošetřené nosičem obsahujícím FGF2-STAB®, vykazovala po 16 týdnech lepší kvalitu v porovnání s kontrolním defektem ošetřeným autologním graftem.
Ověření biokompatibility keramického nosiče in vitro: proliferace hMSC byla měřena jako kvantifikace buněčné DNA (A). Hladina statistické významnosti mezi skupinami je vyznačena nad sloupci (p < 0,05). Buněčná adheze a distribuce na nosiči byla vizualizována pomocí konfokální mikroskopie. Nosič z bifazického kalcium fosfátu (BCP) 1. den po nasazení buněk na nosič (B), bioresorbovatelný hybridní nosič (BHI) v 1. den (C), BCP nosič 14. den (D), BHI nosič 14. den (E). Buněčná jádra byla obarvena propidium jodidem (červená barva), vnitrobuněčné membrány obarveny pomocí DiOC6(3) (zelená barva), měrka 200 µm.
Hodnotili jsme vliv nanotrubiček s průměrem 18, 36 a 46 nm, vytvořených anodickou oxidací na povrchu β-titanové slitiny Ti-36Nb-6Ta, na růst a diferenciaci humánních mezenchymálních kmenových buněk. Nanotrubičky snížily modulus elasticity na hodnotu podobnou hodnotě v kosti, podporovaly adhezi buněk a osteogenní diferenciaci buněk (stimulovaly ALP aktivitu, syntézu kolagenu I a expresi osteokalcinu). Ti-36Nb-6Ta s průměrem nanotrubiček 36 nm je nejnadějnější materiál pro implantaci do kosti.
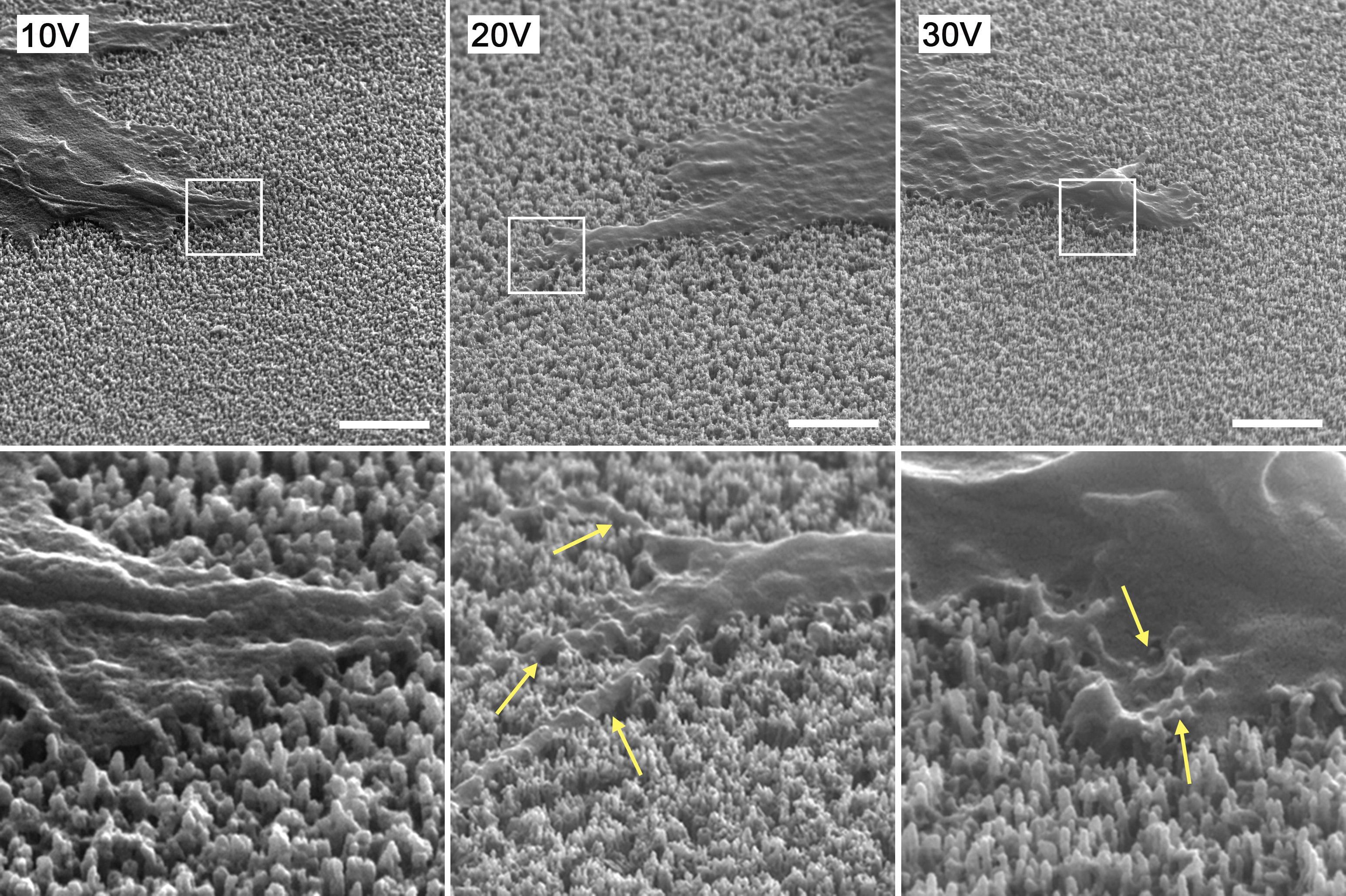
Vizualizace humánních mezenchymálních kmenových buněk adherovaných na nanotrubičky, vytvořené na Ti-36Nb-6Ta anodickou oxidací při 10, 20 a 30 V, 24 hod po nasazení pomocí rastrovacího elektronového mikroskopu
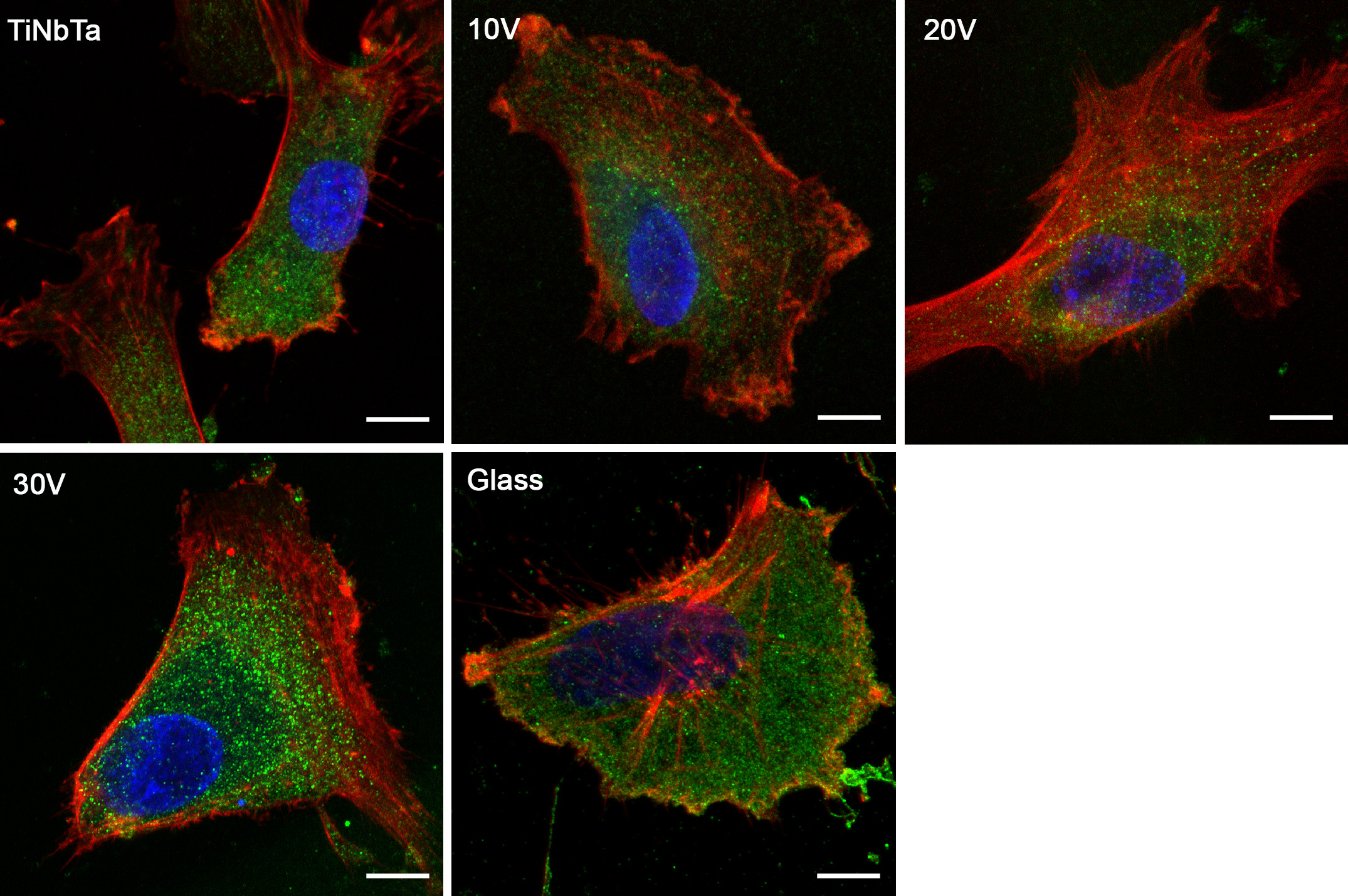
Vizualizace hMSCs adherovaných na β-titanovou slitinu Ti-36Nb-6Ta nanostrukturovanou pomocí anodické oxidace při 10 V, 20 V a 30 V pomocí konfokální mikroskopie
Zabývali jsme se 3D tiskem biokompatibilního nosiče pro regeneraci kostní tkáně na bázi PHB/PLA pomocí FDM technologie. Byly připraveny 4 různé filamenty s trikalciumfosfátem (TCP) a dvěma různými změkčovadly, Citroflex a Syncroflex. Byl sledován vliv těchto aditiv na termální a mechanické vlastnosti materiálu. Dále byl sledován jejich vliv na tisknutelnost, biokompatibilitu a osteogenní diferenciaci mezenchymálních kmenových buněk.
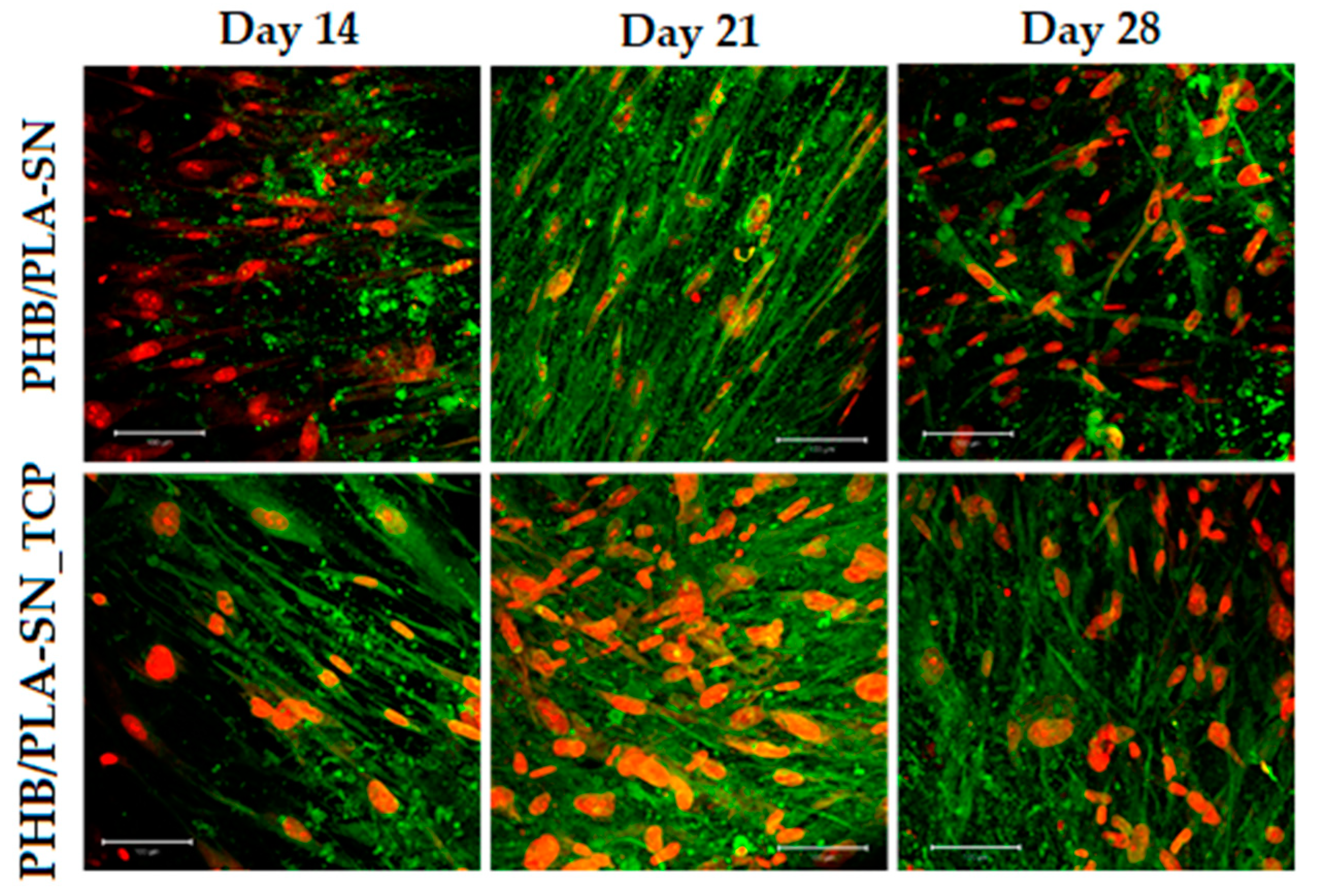
Vizualizace osteokalcinu, proteinu typického pro kostní tkáň, produkovaného buňkami rostoucími na nosiči pomocí konfokální mikroskopie
Testovali jsme pěnové nosiče ze zesíťovaného kolagenu typu I, s přídavkem chitosanu/ Ca soli oxidované celulózy (CaOC)/chitin-chitosan-glukanového komplexu a bovinního lyzátu. Na nosičích s obsahem polysacharidů a bovinního lyzátu byla významně zvýšena metabolická aktivita myších 3T3 fibroblastů. Nosiče obsahující kolagen/chitosan/bovinní lyzát nejlépe podporovaly proliferaci buněk. U nosičů z kolagenu s bovinním lyzátem byl zjištěn pozitivní vliv na angiogenezi v porovnání s čistým kolagenním nosičem.
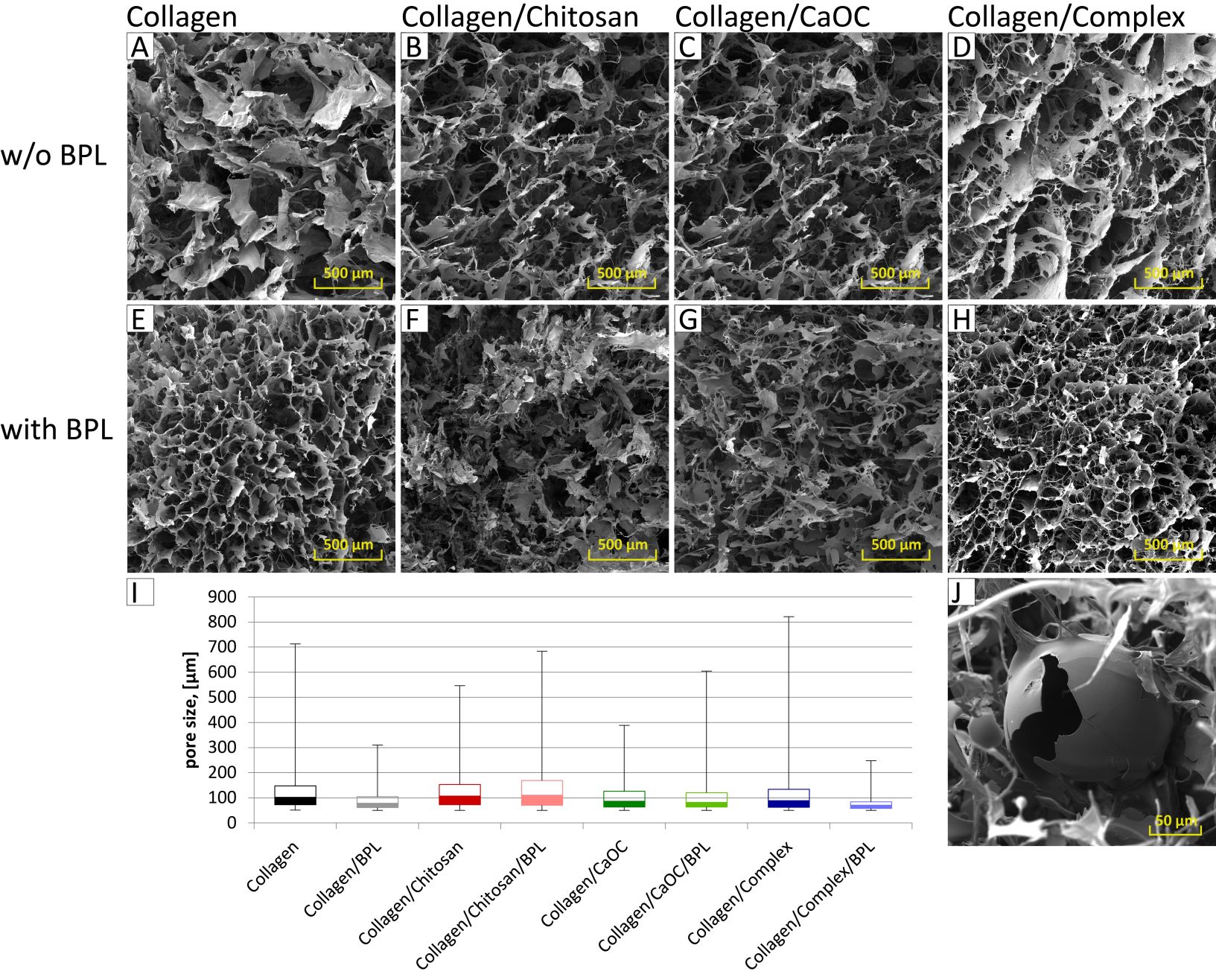
SEM mikrofotografie připravených zesíťovaných pěn s různými aditivy a hodnocení velikosti pórů

Metabolická aktivita (A) a proliferace (B) myších 3T3 fibroblastů na kompozitních kolagenních nosičích
Připravili jsme nosiče z poly-ε-kaprolaktonu pomocí elektrostatického a odstředivého zvlákňování a modifikovali je 5 různými koncentracemi trombocytů. 3D struktura vláken napomohla proliferaci buněk. Po přidání trombocytů se zvyšovala metabolická aktivita, proliferace a tvorba alkalické fosfatázy, a to v závislosti na koncentraci trombocytů. Osteokonduktivní účinek byl dále zvýšen přidáním osteogenních suplementů do kultivačního média.

Nosiče připravené pomocí elektrostatického (ES) a centrifugačního (CS) zvlákňování s adherovanými trombocyty zobrazené pomocí rastrovací elektronové mikroskopie
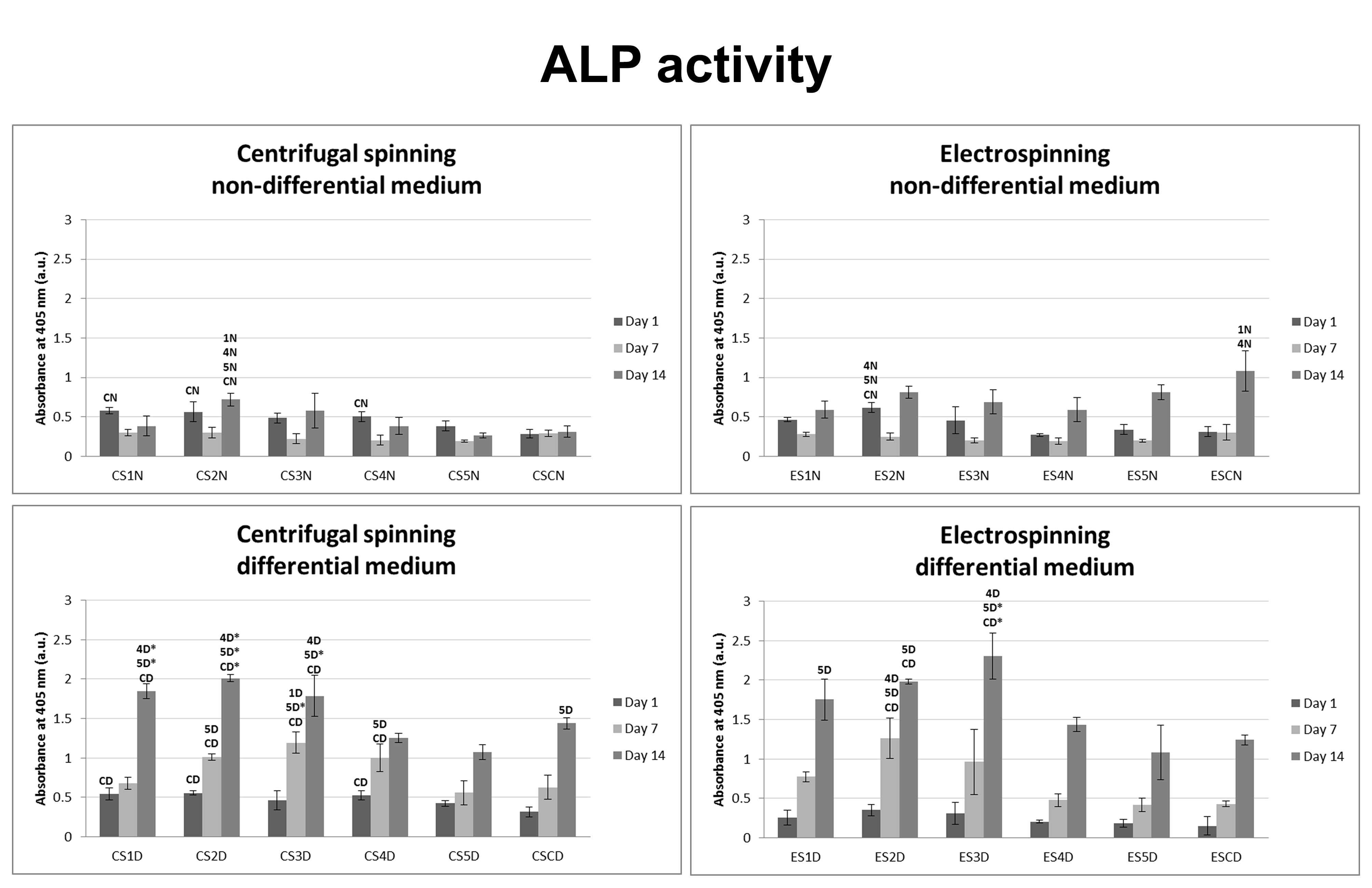
Aktivita alkalické fosfatázy produkované hMSC rostoucích na nosičích připravených elektrostatickým a odstředivým zvlákňováním byla závislá na koncentraci trombocytů
Pomocí počítačového modelování se nám podařilo identifikovat aktivní místo interakce eukaryotického elongačního faktoru 1-α 1 (eEF1A1) s gamendazolem, známým jako potenciální mužská antikoncepce. Na základě této znalosti byla navržena nová série příbuzných látek – derivátů 2-fenyl-3-hydroxy-4(1H)-chinolinonů (3-HQs), které vykazovaly anti-kancerogenní aktivitu. Tyto látky byly syntetizovány a jejich aktivita poté potvrzena pomocí isotermální titrační kalorimetrie, která potvrdila jejich silnou vazbu na eEF1A1. Navíc jsme potvrdili, že některé tyto látky vykázaly signifikantní protirakovinnou aktivitu in vitro.

Aktivní místo interakce eukaryotického elongačního faktoru 1-α 1 (eEF1A1) s gamendazolem. Interakce gamendazolu (červeně) s eEF1A1. Části eEF1A1, které byly již dříve identifikovány jako interagující s gamendazloem jsou označeny zeleně (tyto části byly potvrzeny naším in silico experimentem) a žlutě – tyto části jsme nepotvrdili.
Připravili jsme kompozitní nosič ze standardní polypropylenové síťky a vrstvy nanovláken z poly- ε-kaprolaktonu (PCL) a testovali jej na modelu incisionální hernie velkého zvířecího modelu (miniaturní prase). Histologické a biomechanické měření ukázalo, že přítomnost PCL nanovláken vedla k přerůstání tkáně a tvorbě tlusté fibrózní vrstvy kolem implantátu. Současně byla urychlena maturace kolagenu a jizva byla více flexibilní a elastická než u vzorků se samotnou polypropylenovou síťkou. U kompozitního nosiče bylo také pozorováno menší smršťování jizvy. Kompozitní nosiče však byly méně odolné při namáhání v tahu než samotná polypropylenová síťka.
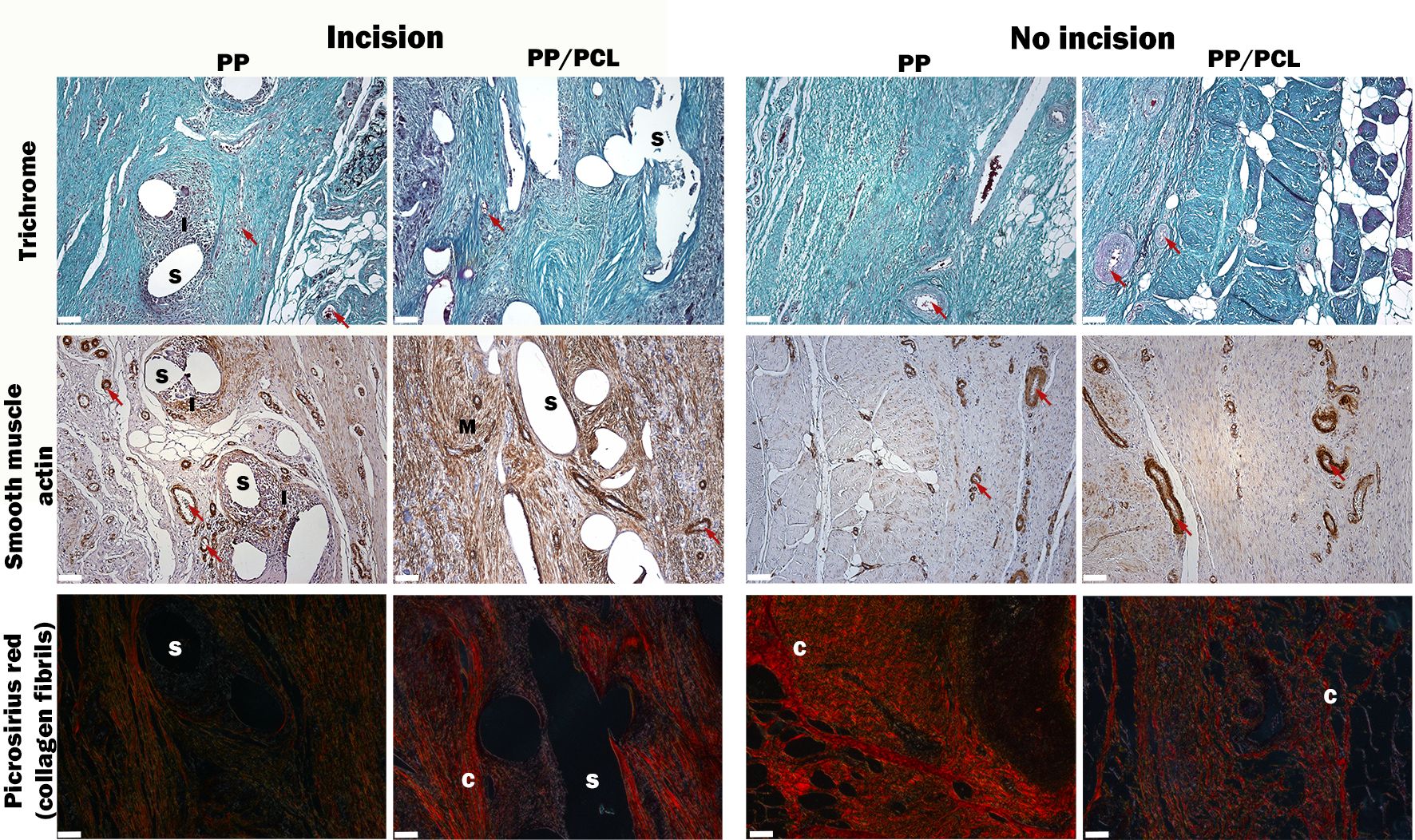
Histologické hodnocení incize a oblasti bez incize. Stehy (S) byly obklopeny infiltrovanými zánětlivými buňkami (I). V oblasti incize vzorky PP/PCL obsahovaly nižší počet cév pozitivních na aktin (červené šipky), vyšší frakci myofibroblastů pozitivních na aktin (M) a kolagen typu I (C)
Terapie s NZ snížila migraci a diferenciaci MSCs do adipocytů a osteoblastů a inhibovala sekreci proangiogenních faktorů. NZ byla schopna inhibovat interakci mezi MSCs a PCa, což vysvětluje protirakovinné účinky NZ na PCa. (Borghese et al. 2017)
Kultivace MSC s nanočásticemi obsahujícími zoledronovou kyselinu (NZ) nebo roztokem zoledronové kyseliny (ZA) snížila klonogenní růst buněk rakoviny prostaty (PC3 buněk) indukovaný kondicionovaným médiem MSC (MSC-CM)
Třírozměrná PCL vlákna byla připravena pomocí centrifugačního zvlákňování a byla funkcionalizována pomocí adherovaných krevných destiček 5 různých koncentrací. Uvolněné růstové faktory stimulovali proliferaci a metabolickou aktivitu MG-63 buněk v koncentraci destiček větší než fyziologické (300×109/l). Nižší koncentrace byly srovnatelné s kontrolní skupinou. Podobně i aktivita alkalické fosfatázy byla zvýšena u dvou nosičů s 2 nejvyššími koncentracemi destiček. (Rampichová et al. 2017)
Krevní destičky adherovaná na vlákna z poly- ε-kaprolaktonu
Studie porovnává bioaktivní peptidy odvozené z proteinů extracelulární matrix, jmenovitě kolagen typu III, BMP-7 and BMP-2. Peptid odvozený z BMP-2 má nejvyšší potenciál navodit osteogenní diferenciaci kultivovaných pMSC. (Lukasova et al. 2017)
Exprese genu pro osteokalcin
Nanovlákna zlepšila adhezi a osteogenní proliferaci prasečích mesenchymálních kmenových buněk a jsou slibná pro kostní regeneraci. (Daňková et al. 2015).
Rastrovací elektronová mikroskopie nanovláken z poly-ε-kaprolaktonu s magnetickými nanočásticemi.
Složená síťka s trombocyty zlepšila adhezi, proliferaci a metabolickou aktivitu fibroblastů v porovnání s PP, PP obaleným nanovlákny a PP funkcionalizovaným trombocyty. Systém složených nosičů s růstovými faktory uvolněnými z trombocytů je slibný přístup pro tkáňové inženýrství (Plencner et al. 2015).
Rastrovací elektronová mikroskopie implantovaných nosičů. (A) PCL nanovlákna; (B) PP síťka; (C) PP síťka funkcionalizovaná PCL nanovlákny.
PEG-b funkcionalizovaná nanovlákna signifikantně řízeně zpomalila rozpad nanovláken. Navíc vazby anti CD-29 protilátky na PEG-b linker stimulovala adhezi mesenchymálních kmenových buněk na PVA-PEG-b nanovlákna přes β1-integrinový receptor. Druhý systém selektivní vazby proteinu na povrch nanovláken představují anti-transferrin-PEG-b nanovlákna (Buzgo et al. 2015).
Mikrofotografie a schéma nanovláken z polyvinylalkoholu (PVA) funkcionalizovaných linkerem polyetylénglykolem s biotinem (PEG-b) a sekvenčne-specifickou vazbou konjugátu avidin- protilátka (proti-transferinu).
Polypropylenová síťka byla funkcionalizována pomocí nanovláken z poly-ε-kaprolaktonu s adherovanými bioaktivními látkami jako systém pro řešení incisionální hernie. Tento systém funkcionalizovaných nanovláken s řízeným dodáváním bioaktivních látek byl následně testován in vivo na modelu králíka.
Scaffold pro krytí břišních ran pomocí skenovací elektronové mikroskopie. (A) nanovlákna z poly-ε-kaprolaktonu (zvětšení 230×); (B) polypropylenová síťka (zvětšení 18×); (C) polypropylenová síťka funkcionalizovaná poly-ε-kaprolaktonovými nanovlákny (zvětšení 18×)
Uzavření břišní stěny bylo zpevněno aplikací polypropylenové síťky funcionalizované pomocí nanovláken z poly-ε-kaprolaktonu (PCL) a růstových faktorů. Tento nový přistup je použitý jako prevence vzniku incizionální kýly. Jelikož je tento systém velice obecný je možné ho využít i v dalších mnohých chirurgických aplikacích.
Snímky nosičů použitých pro uzavření břišní incize pořízené pomocí skenovací elektronové mikroskopie (SEM). (A) PCL nanovlákna (230 × zvětšené), (B) polypropylénová síťka (18 × zvětšené), (C) polypropylénová síťka funcionalizována pomocí PCL nanovláken (18 × zvětšené).
Histologické vyšetření vzorků nosičů pomocí barvení kolagenu, tukové tkáně a granulačních infiltrací. Ve vzorcích bez použití jakékoliv síťky (A) byla v hojící se incizi přítomná směs kolagenů (červená šipka), tuková pojivová tkáň (černá šipka) a granulační infiltrace (žlutá šipka). Vzorky s polypropylénovou (PP) síťkou (B) vykazovali přítomnost vyšší frakce tukové tkáně. Na snímku B můžeme taky pozorovat pozůstatky rozpuštěné PP síťky (černé šipky), které byly obklopeny pouze několika pro-zápalovými buňkami. Zbytky nanovláken (C, D, E, F) byly obklopeny granulační, na leukocyty bohatou, pojivovou tkání (žlutá šipka). Největší frakce kolagenu (červená šipka) byla pozorována ve vzorcích obsahujících PCL nanovlákna s adherovanými růstovými faktory (RF)(D), následovaných vzorky bez použití jakékoliv síťky (A) a vzorky s použitím samotných PCL nanovláken (F). Nízká frakce tukové tkáně byla pozorována ve vzorcích obsahujících PCL nanovlákna s adherovanými RF (D), ve vzorcích bez použití síťky (A), a ve vzorcích obsahujících samotná PCL nanovlákna (F).
Alfa granule přinášejí nový zdroj přirozených růstových faktorů z krevních destiček. V posledních studiích se nám podařilo úspěšně zapouzdřit tyto alfa granule do koaxiálních nanovláken (nanovlákna typu jádro/plášť). Alfa granule přežily proces elektrostatického zvlákňování. Bioaktivita růstových faktorů uvolňujících se ze zapouzdřených alfa granulí byla prokázána in vitro na primárních buňkách chrupavčité tkáně (chondrocytech) a mezenchymálních kmenových buňkách.
Mikrofotografie alfa-granul enkapsulovaných v koaxiálních nanovláknech z polykaprolaktonu a polyvinyl alkoholu pomocí rastrovací elektronové mikroskopie (FESEM).
Byl vyvinut nový systém pro dodávání léčiv založený na liposomech enkapsulovaných do PVA nanovláken. Časová kontrola uvolňování insulinu a bFGF zlepšila viabilitu mesenchymálních kmenových buněk MSC in vitro. Bezbuněčné kompozitní nosiče složené z PVA nanovláken obohacených o liposomy, bFGF a insulin byly implantovány do 7 osteochondrálních defektů v modelu miniprasete; kontrolní defekty nebyly léčeny. Bezbuněčný kompozitní nosič zvýšil migraci buněk do defektu a jejich diferenciaci do chondrocytů. Nosič podpořil regeneraci osteochondrálních defektů na modelu miniprasete.
Regenerace osteochondrálního defektu u miniprasete pomocí bezbuněčného gelu složeného z kolagenu typu I/hyalurona- nu sodného/fibrinu, obsahující nanovlákna z polyvinylalkoholu obohacená o lipozomy a růstové faktory A. a neléčený defekt B.
Alfa-granula krevních destiček jsou novým, přirozeným zdrojem růstových faktorů. Naše skupina v nedávné době úspěšně inkorporovala alfa-granula do nanovláken typu jádro/plášť. Pomocí chondrocytů a mesenchymálních kmenových buněk bylo prokázáno, že elektrostatické zvlákňování nenarušuje bioaktivitu uzavřených růstových faktorů.
Koaxiální nanovlákna z polyvinyl alkoholu (jádro) a polykaprolaktonu (plášť) s inkorporovanými alfa-granulemi značenými carboxyfluorescein succinimidyl esterom snímané konfokálním mikroskopem.
Daniel, M., Eleršič Filipič, K., Filová, E., Judl, T., & Fojt, J. (2022). Modelling the role of membrane mechanics in cell adhesion on titanium oxide nanotubes. Computer methods in biomechanics and biomedical engineering, 1–10. Advance online publication. https://doi.org/10.1080/10255842.2022.2058875
Hefka Blahnová, V. , Vojtová, L., Pavliňáková, V., Muchová, J., & Filová, E. (2022). Calcined Hydroxyapatite with Collagen I Foam Promotes Human MSC Osteogenic Differentiation. International journal of molecular sciences, 23(8), 4236. https://doi.org/10.3390/ijms23084236
Nirwan, V. P., Kowalczyk, T., Bar, J., Buzgo, M., Filová, E., & Fahmi, A. (2022). Advances in Electrospun Hybrid Nanofibers for Biomedical Applications. Nanomaterials (Basel, Switzerland), 12(11), 1829. https://doi.org/10.3390/nano12111829
Žižková, R. , Hedvičáková, V., Blahnová, V. H., Sovková, V., Rampichová, M., & Filová, E. (2022). The Effect of Osteoblast Isolation Methods from Adult Rats on Osteoclastogenesis in Co-Cultures. International journal of molecular sciences, 23(14), 7875. https://doi.org/10.3390/ijms23147875
Hedvičáková, V. , Žižková, R., Buzgo, M., Rampichová, M., & Filová, E. (2021). The Effect of Alendronate on Osteoclastogenesis in Different Combinations of M-CSF and RANKL Growth Factors. Biomolecules, 11(3), 438. https://doi.org/10.3390/biom11030438
Zhu, H., Blahnová, V. H., Perale, G., Xiao, J., Betge, F., Boniolo, F., Filová, E., Lyngstadaas, S. P., & Haugen, H. J. (2020). Xeno-Hybrid Bone Graft Releasing Biomimetic Proteins Promotes Osteogenic Differentiation of hMSCs. Frontiers in cell and developmental biology, 8, 619111. https://doi.org/10.3389/fcell.2020.619111
Frtús, A., Smolková, B., Uzhytchak, M., Lunova, M., Jirsa, M., Hof, M., Jurkiewicz, P., Lozinsky, V. I., Wolfová, L., Petrenko, Y., Kubinová, Š., Dejneka, A., & Lunov, O. (2020). Hepatic Tumor Cell Morphology Plasticity under Physical Constraints in 3D Cultures Driven by YAP-mTOR Axis. Pharmaceuticals (Basel, Switzerland), 13(12), 430. https://doi.org/10.3390/ph13120430
Krticka, M., Planka, L., Vojtova, L., Nekuda, V., Stastny, P., Sedlacek, R., Brinek, A., Kavkova, M., Gopfert, E., Hedvicakova, V., Rampichova, M., Kren, L., Liskova, K., Ira, D., Dorazilová, J., Suchy, T., Zikmund, T., Kaiser, J., Stary, D., Faldyna, M., … Trunec, M. (2021). Lumbar Interbody Fusion Conducted on a Porcine Model with a Bioresorbable Ceramic/Biopolymer Hybrid Implant Enriched with Hyperstable Fibroblast Growth Factor 2. Biomedicines, 9(7), 733. https://doi.org/10.3390/biomedicines9070733
Sovkova, V. , Vocetkova, K., Hedvičáková, V., Hefka Blahnová, V., Buzgo, M., Amler, E., & Filová, E. (2021). Cellular Response to Individual Components of the Platelet Concentrate. International journal of molecular sciences, 22(9), 4539. https://doi.org/10.3390/ijms22094539
Vojtová, L., Pavliňáková, V., Muchová, J., Kacvinská, K., Brtníková, J., Knoz, M., Lipový, B., Faldyna, M., Göpfert, E., Holoubek, J., Pavlovský, Z., Vícenová, M., Blahnová, V. H., Hearnden, V., & Filová, E. (2021). Healing and Angiogenic Properties of Collagen/Chitosan Scaffolds Enriched with Hyperstable FGF2-STAB® Protein: In Vitro, Ex Ovo and In Vivo Comprehensive Evaluation. Biomedicines, 9(6), 590. https://doi.org/10.3390/biomedicines9060590
Nirwan, V. P., Filova, E., Al-Kattan, A., Kabashin, A. V., & Fahmi, A. (2021). Smart Electrospun Hybrid Nanofibers Functionalized with Ligand-Free Titanium Nitride (TiN) Nanoparticles for Tissue Engineering. Nanomaterials (Basel, Switzerland), 11(2), 519. https://doi.org/10.3390/nano11020519
Hefka Blahnova, V., Dankova, J., Rampichova, M., & Filova, E. (2020). Combinations of growth factors for human mesenchymal stem cell proliferation and osteogenic differentiation. Bone & joint research, 9(7), 412–420.
Jarolimova, P., Voltrova, B., Blahnova, V., Sovkova, V., Pruchova, E., Hybasek, V., Fojt, J., Filova, E. (2020). Mesenchymal stem cell interaction with Ti6Al4V alloy pre-exposed to simulated body fluid. RSC ADVANCES, 10(12), 6858-6872
Voltrova, B., Jarolimova, P., Hybasek, V., Blahnova, V. H., Sepitka, J., Sovkova, V., Matějka, R., Daniel, M., Fojt, J., & Filova, E. (2020). In vitro evaluation of a novel nanostructured Ti-36Nb-6Ta alloy for orthopedic applications. Nanomedicine (London, England), 15(19), 1843–1859.
Filová, E., Tonar, Z., Lukášová, V., Buzgo, M., Litvinec, A., Rampichová, M., Beznoska, J., Plencner, M., Staffa, A., Daňková, J., Soural, M., Chvojka, J., Malečková, A., Králíčková, M., & Amler, E. (2020). Hydrogel Containing Anti-CD44-Labeled Microparticles, Guide Bone Tissue Formation in Osteochondral Defects in Rabbits. Nanomaterials (Basel, Switzerland), 10(8), 1504.
Vocetkova, K., Sovkova, V., Buzgo, M., Lukasova, V., Divin, R., Rampichova, M., Blazek, P., Zikmund, T., Kaiser, J., Karpisek, Z., Amler, E., & Filova, E. (2020). A Simple Drug Delivery System for Platelet-Derived Bioactive Molecules, to Improve Melanocyte Stimulation in Vitiligo Treatment. Nanomaterials (Basel, Switzerland), 10(9), 1801.
Melčová, V., Svoradová, K., Menčík, P., Kontárová, S., Rampichová, M., Hedvičáková, V., Sovková, V., Přikryl, R., & Vojtová, L. (2020). FDM 3D Printed Composites for Bone Tissue Engineering Based on Plasticized Poly(3-hydroxybutyrate)/poly(d,l-lactide) Blends. Polymers, 12(12), 2806.
Zhu, H., Blahnová, V. H., Perale, G., Xiao, J., Betge, F., Boniolo, F., Filová, E., Lyngstadaas, S. P., & Haugen, H. J. (2020). Xeno-Hybrid Bone Graft Releasing Biomimetic Proteins Promotes Osteogenic Differentiation of hMSCs. Frontiers in cell and developmental biology, 8, 619111.
Frtús, A., Smolková, B., Uzhytchak, M., Lunova, M., Jirsa, M., Hof, M., Jurkiewicz, P., Lozinsky, V. I., Wolfová, L., Petrenko, Y., Kubinová, Š., Dejneka, A., & Lunov, O. (2020). Hepatic Tumor Cell Morphology Plasticity under Physical Constraints in 3D Cultures Driven by YAP-mTOR Axis. Pharmaceuticals (Basel, Switzerland), 13(12), 430.
Vojtova, L., Michlovska, L., Valova, K., Zboncak, M., Trunec, M., Castkova, K., Krticka, M., Pavlinakova, V., Polacek, P., Dzurov, M., Lukasova, V., Rampichova, M., Suchy, T., Sedlacek, R., Ginebra, M. P., & Montufar, E. B. (2019). The Effect of the Thermosensitive Biodegradable PLGA⁻PEG⁻PLGA Copolymer on the Rheological, Structural and Mechanical Properties of Thixotropic Self-Hardening Tricalcium Phosphate Cement. International journal of molecular sciences, 20(2), 391.
Buzgo, M., Plencner, M., Rampichova, M., Litvinec, A., Prosecka, E., Staffa, A., Kralovic, M., Filova, E., Doupnik, M., Lukasova, V., Vocetkova, K., Anderova, J., Kubikova, T., Zajicek, R., Lopot, F., Jelen, K., Tonar, Z.,Amler, E., Divin, R., Fiori, F. (2019). Poly-ε-caprolactone and polyvinyl alcohol electrospun wound dressings: adhesion properties and wound management of skin defects in rabbits. Regenerative Medicine.14(5):423-445.
Stastny, P., Sedlacek, R., Suchy, T., Lukasova, V., Rampichova, M., & Trunec, M. (2019). Structure degradation and strength changes of sintered calcium phosphate bone scaffolds with different phase structures during simulated biodegradation in vitro. Materials science & engineering. C, Materials for biological applications, 100, 544–553.
Lukášová, V., Buzgo, M., Vocetková, K., Sovková, V., Doupník, M., Himawan, E., Staffa, A., Sedláček, R., Chlup, H., Rustichelli, F., Amler, E., & Rampichová, M. (2019). Needleless electrospun and centrifugal spun poly-ε-caprolactone scaffolds as a carrier for platelets in tissue engineering applications: A comparative study with hMSCs. Materials science & engineering. C, Materials for biological applications, 97, 567–575.
Voltrova, B., Hybasek, V., Blahnova, V., Sepitka, J., Lukasova, V., Vocetkova, K., Sovkova, V., Matejka, R., Fojt, J., Joska, L., Daniel, M., Filova, E. (2019). Different diameters of titanium dioxide nanotubes modulate Saos-2 osteoblast-like cell adhesion and osteogenic differentiation and nanomechanical properties of the surface. RSC ADVANCES 9(20), 11341-11355.
East, B., Plencner, M., Otahal, M., Amler, E., & de Beaux, A. C. (2019). Dynamic creep properties of a novel nanofiber hernia mesh in abdominal wall repair. Hernia : the journal of hernias and abdominal wall surgery, 23(5), 1009–1015.
Babrnáková, J., Pavliňáková, V., Brtníková, J., Sedláček, P., Prosecká, E., Rampichová, M., Filová, E., Hearnden, V., & Vojtová, L. (2019). Synergistic effect of bovine platelet lysate and various polysaccharides on the biological properties of collagen-based scaffolds for tissue engineering: Scaffold preparation, chemo-physical characterization, in vitro and ex ovo evaluation. Materials science & engineering. C, Materials for biological applications, 100, 236–246.
Horakova, J., Mikes, P., Lukas, D., Saman, A., Jencova, V., Klapstova, A., Svarcova, T., Ackermann, M., Novotny, V., Kalab, M., Lonsky, V., Bartos, M., Rampichova, M., Litvinec, A., Kubikova, T., Tomasek, P., & Tonar, Z. (2018). Electrospun vascular grafts fabricated from poly(L-lactide-co-ε-caprolactone) used as a bypass for the rabbit carotid artery. Biomedical materials (Bristol, England), 13(6), 065009.
Alaia, C., Boccellino, M., Zappavigna, S., Amler, E., Quagliuolo, L., Rossetti, S., Facchini, G., & Caraglia, M. (2018). Ipilimumab for the treatment of metastatic prostate cancer. Expert opinion on biological therapy, 18(2), 205–213.
Zaviskova, K., Tukmachev, D., Dubisova, J., Vackova, I., Hejcl, A., Bystronova, J., Pravda, M., Scigalkova, I., Sulakova, R., Velebny, V., Wolfova, L., & Kubinova, S. (2018). Injectable hydroxyphenyl derivative of hyaluronic acid hydrogel modified with RGD as scaffold for spinal cord injury repair. Journal of biomedical materials research. Part A, 106(4), 1129–1140.
Burglová, K., Rylová, G., Markos, A., Prichystalova, H., Soural, M., Petracek, M., Medvedikova, M., Tejral, G., Sopko, B., Hradil, P., Dzubak, P., Hajduch, M., & Hlavac, J. (2018). Identification of Eukaryotic Translation Elongation Factor 1-α 1 Gamendazole-Binding Site for Binding of 3-Hydroxy-4(1 H)-quinolinones as Novel Ligands with Anticancer Activity. Journal of medicinal chemistry, 61(7), 3027–3036.
East, B., Plencner, M., Kralovic, M., Rampichova, M., Sovkova, V., Vocetkova, K., Otahal, M., Tonar, Z., Kolinko, Y., Amler, E., & Hoch, J. (2018). A polypropylene mesh modified with poly-ε-caprolactone nanofibers in hernia repair: large animal experiment. International journal of nanomedicine, 13, 3129–3143.
Lukasova, V., Buzgo, M., Vocetkova, K., Kubikova, T., Tonar, Z., Doupnik, M., Blahnova, V., Litvinec, A., Sovkova, V., Voltrova, B., Staffa, A., Svora, P., Kralickova, M., Amler, E., Filova, E., Rustichelli, F., Rampichova, M. (2018) Osteoinductive 3D scaffolds prepared by blend centrifugal spinning for long-term delivery of osteogenic supplements. RSC ADVANCES, 8(39), 21889-21904
Borghese, C., Casagrande, N., Pivetta, E., Colombatti, A., Boccellino, M., Amler, E., Normanno, N., Caraglia, M., De Rosa, G., Aldinucci, D.: (2017) Self-assembling nanoparticles encapsulating zoledronic acid inhibit mesenchymal stromal cells differentiation, migration and secretion of proangiogenic factors and their interactions with prostate cancer cells. OncoTarget. 8 (26): 42926-42938.
Buzgo, M., Rampichová, M., Vocetková, K., Sovková, V., Lukášová, V., Doupnik, M., Míčková, A., Rustichelli, F., Amler, E.: (2017) Emulsion centrifugal spinning for production of 3D drug releasing nanofibres with core/shell structure. RSC Advances. 7(3): 1215-1228.
Buzgo, M., Filová, E., Staffa, A., Rampichová, M. , Doupnik, M., Vocetková, K., Lukášová, V., Kolcun, R., Lukáš, D., Nečas, A., Amler, E.: (2017) Needleless emulsion electrospinning for the regulated delivery of susceptible proteins. Journal of Tissue Engineering and Regenerative Medicine. May 16. doi: 10.1002/term.2474. [Epub ahead of print]
Gregor, A., Filová, E., Novák, M., Kronek, J., Chlup, H., Buzgo, M., Blahnová, V., Lukášová, V., Bartoš, M., Nečas, A., Hošek, J.: (2017) Designing of PLA scaffolds for bone tissue replacement fabricated by ordinary commercial 3D printer. Journal of Biological Engineering. 11: 31.
Hadraba, D., Janáček, J., Filová, E., Lopot, F., Paesen, R., Fanta, O., Jarman, A., Nečas, A., Ameloot, M., Jelen, K.: (2017) Calcaneal Tendon Collagen Fiber Morphometry and Aging. Microscopy and Microanalysis. 23 (5): 1040-1047.
Lukášová, V., Buzgo, M., Sovková, V., Daňková, J., Rampichová, M., Amler, E.: (2017) Osteogenic differentiation of 3D cultured mesenchymal stem cells induced by bioactive peptides. Cell Proliferation. 50 (4): e12357.
Paino, F., Noce, M.L., Giuliani, A., de Rosa, A., Mazzoni, F., Laino, L., Amler, E., Papaccio, G., Desiderio, V., Tirino, V.: (2017) Human DPSCs fabricate vascularized woven bone tissue: A new tool in bone tissue engineering. Clinical science. 131(8): 699-713.
Rampichová, M., Buzgo, M., Míčková, A., Vocetková, K., Sovková, V., Lukášová, V., Filová, E., Rustichelli, F., Amler, E.: (2017) Platelet-functionalized three-dimensional polye-epsilon-caprolactone fibrous scaffold prepared using centrifugal spinning for delivery of growth factors. International Journal of Nanomedicine. 12:347-361.
Rampichová, M. , Chvojka, J., Jenčová, V., Kubíková, T., Tonar, Z., Erben, J., Buzgo, M., Daňková, J., Litvinec, A., Vocetková, K., Plencner, M., Prosecká, E., Sovková, V., Lukášová, V., Králíčková, M., Lukáš, D., Amler, E.: (2017) The combination of nanofibrous and microfibrous materials for enhancement of cell infiltration and in vivo bone tissue formation. Biomedical Materials. IN PRESS
Rampichová, M. , Kuželová Košťáková, E., Filová, E., Chvojka, J., Šafka, J., Pelcl, M., Daňková, J., Prosecká, E., Buzgo, M., Plencner, M., Lukáš, D., Amler, E.: (2017) Composite 3D printed scaffold with structured electrospun nanofibers promotes chondrocyte adhesion and infiltration. Cell Adhesion and Migration. Nov 13:1-15. doi: 10.1080/19336918.2017.1385713. [Epub ahead of print]
Sovková, V., Vocetková, K., Rampichová, M., Míčková, A., Buzgo, M., Lukášová, V., Daňková, J., Filová, E. , Nečas, A., Amler, E.: (2017) Platelet lysate as a serum replacement for skin cell culture on biomimetic PCL nanofibers. Platelets. Jun 26:1-11. doi: 10.1080/09537104.2017.1316838. [Epub ahead of print]
Szöke, K., Daňková, J., Buzgo, M., Amler, E., Brinchmann, J.E., Østrup, E.: (2017) The effect of medium composition on deposition of collagen type 1 and expression of osteogenic genes in mesenchymal stem cells derived from human adipose tissue and bone marrow. Process Biochemistry. 59(B): 321-328.
Tejral, G., Sopko, B., Nečas, A., Schoner, W., Amler, E.: (2017) Computer modelling reveals new conformers of the ATP binding loop of Na+/K+-ATPase involved in the transphosphorylation process of the sodium pump. PeerJ. 5: 3087.
Vocetková, K. , Buzgo, M., Sovková, V., Rampichová, M., Staffa, A., Filová, E., Lukášová, V., Doupnik, M., Fiori, F., Amler, E.: (2017) A comparison of high throughput core–shell 2D electrospinning and 3D centrifugal spinning techniques to produce platelet lyophilisate-loaded fibrous scaffolds and their effects on skin cells. RSC Advances. 7(85): 53706-53719.
Vysloužilová, L., Buzgo, M., Pokorný, P., Chvojka, J., Míčková, A., Rampichová, M., Kula, J., Pejchar, K., Bílek, M., Lukáš, D., Amler, E.: (2017) Needleless coaxial electrospinning: A novel approach to mass production of coaxial nanofibers. International Journal of Pharmaceutics. 516(1-2):293-300.
Smyslová, P., Popa, I., Lyčka, A., Tejral, G., Hlaváč, J.:(2016) Non-Catalyzed Click Reactions of ADIBO Derivatives with 5-Methyluridine Azides and Conformational Study of the Resulting Triazoles. PLoS One., 10(12): e0144613.
Filová, E., Jakubcová, B. , Danilová, I., Kuželová Košťáková, E., Jarošíková, T., Chernyavskiy, O., Hejda, J., Handl, M., Beznoská, J., Nečas, A., Rosina, J., Amler, E.: (2016) Polycaprolactone foam functionalized with chitosan microparticles - a suitable scaffold for cartilage regeneration. Physiol. Res., 65(1): 121-131.
Vocetková, K., Buzgo, M., Sovková, V., Bezděková, D.
, Kneppo, P., Amler, E.: (2016) Nanofibrous polycaprolactone scaffolds with adhered platelets stimulate proliferation of skin cells. Cell Prolif., 49(5):568-78.
Buzgo, M., Greplová, J., Soural, M., Bezděková, D., Míčková, A., Kofroňová, O., Benada, O., Hlaváč, J., Amler, E.: (2015) PVA immunonanofibers with controlled decay. Polymer. 7: 387-398.
Daňková, J., Buzgo, M., Vejpravová, J., Kubíčková, S., Sovková, V., Vysloužilová, L., Mantlíková, A., Nečas, A., Amler, E.: Highly efficient mesenchymal stem cell proliferation on poly-ε-caprolactone nanofibers with embedded magnetic nanoparticles. Int J Nanomedicine. 10:7307-17.
Erben, J., Pilarová, K., Sanetrnik, F., Chvojka, J., Jenčová, V., Blažková, L., Havlíček, J., Novák, O., Mikeš, P., Prosecká, E., Lukaš, D., Kuzelová Kostaková E.: (2015) The combination of meltblown and electrospinning for bone tissue engineering. Materials Letters 143, 172-176.
Filová, E., Jakubcová, B., Danilová, I., Kuželová Košťáková, E., Jarošíková, T., Chernyavskiy, O., Hejda, J., Handl, M., Beznoská, J., Nečas, A., Rosina, J., Amler, E.: (2015) Polycaprolactone foam functionalized with chitosan microparticles - a suitable scaffold for cartilage regeneration. Physiol Res. IN PRESS
Kubíková, T., Filová, E., Prosecká, E., Plencner, M., Králíčková, M., Tonar, Z.: (2015) Histological evaluation of biomaterials administration in vivo on the cartilage, bone and skin healing. Cas Lek Cesk., 154(3):110-4.
Plencner, M., Prosecká, E., Rampichová, M., East, B., Buzgo, M., Vysloužilová, L., Hoch, J., Amler, E.: (2015) Significant improvement of biocompatibility of polypropylene mesh for incisional hernia repair by using poly-ε-caprolactone nanofibers functionalized with thrombocyte-rich solution. Int J Nanomedicine.10:2635-2646.
Prosecká, E., Rampichová, M., Litvinec, A., Tonar, Z., Králíčková, M., Vojtová, L., Kochová, P., Plencner, M., Buzgo, M., Míčková, A., Jančář, J., Amler, E.: (2015) Collagen/hydroxyapatite scaffold enriched with polycaprolactone nanofibers, thrombocyte-rich solution and mesenchymal stem cells promotes regeneration in large bone defect in vivo. J. Biomed. Mater. Res. Part A., 103(2): 671-682.
Sukhoruková, I.V., Sheveyko, A.N., Kiryukhantsev-Korneev,Ph.V., AnisimováN.Y., Gloushanková, N.A., Zhitnyak, I.Y., Benešová, J., Amler, E., Shtanský, D.V.: (2015) Two approaches to form antibacterial surface: Doping with bactericidal element and drug loading. Applied Surface Science. 330:339–350.
Amler, E., Filová, E., Buzgo, M., Prosecká, E., Rampichová, M., Nečas, A., Nooeaid, P., Boccaccini, A. R.: (2014) Functionalized nanofibers as drug-delivery systems for osteochondral regeneration. Nanomedicine-UK 9(7): 1083-1094.
Fedorová, P., Srnec, R., Pěnčík, J., Schmid, P., Amler, E., Urbanová, L., Nečas, A.: (2014) Mechanical testing of newly developed biomaterial designed for intra-articular reinforcement of partially ruptured cranial cruciate ligament: ex vivo pig model. Acta Vet.BRNO 83(1): 55-60.
Plencner, M., East, B., Tonar, Z., Otáhal, M., Prosecká, E., Rampichová, M., Krejčí, T., Litvinec, A., Buzgo, M., Míčková, A., Nečas, A., Hoch, J., Amler, E.: (2014) Abdominal closure reinforcement by using polypropylene mesh functionalized with poly-ε-caprolactone nanofibers and growth factors for prevention of incisional hernia formation. Int. J. Nanomed. 9: 3263-3277.
Rampichová, M., Buzgo, M., Chvojka, J., Prosecká, E., Kofroňová, O., Amler, E.: (2014) Cell penetration to nanofibrous scaffolds: Forcespinning®, an alternative approach for fabricating 3D nanofibers. Celll Adhes. Migr. 8(1): 36-41.
Amler, E., Míčková, A., Buzgo, M.: (2013) Electrospun core/shell nanofibers: a promising system for cartilage and tissue engineering? Nanomedicine-UK. 8(4): 509-512.
Buzgo, M., Jakubová, R., Míčková, A., Rampichová, M., Prosecká, E., Kochová, P., Lukas, D., Amler, E.: (2013) Time-regulated drug delivery system based on coaxially incorporated platelet alpha granules for biomedical use. Nanomedicine-UK. 8(7): 1137-1154.
Filová, E., Rampichová M., Litvinec, A., Držík, M., Míčková, A., Buzgo, M., Košťáková, E., Martinová, L., Usvald, D., Prosecká, E., Uhlík, J., Motlík, J., Vajner, L., Amler, E.: (2013) A cell-free nanofiber composite scaffold regenerated osteochondral defects in miniature pigs. Int. J. Pharm. 447(1-2): 139-149.
Rampichová, M., Chvojka, J., Buzgo, M., Prosecká, E., Mikeš, P., Vysloužilová, L., Tvrdik, D., Kochová, P., Gregor, T., Lukáš, D.,Amler, E.: (2013) Elastic three-dimensional poly (ε-caprolactone) nanofibre scaffold enhanced migration, proliferation, and osteogenic differentiation of mesenchymal stem cells. Cell Prolif. 46(1): 23-37.
Grantová agentura České republiky 18-09306S (2018-2020) Vytvoření pokročilých 3D in vitro modelů osteoporózy a zkoumání mechanizmu osteointegrace biomateriálů pro kostní regeneraci
Ministerstvo průmyslu a obchodu České republiky FV30086 (2018-2021) Kryty ran s antioxidační a antibakteriální funkcí pro hojení chronických ran
Ministerstvo průmyslu a obchodu České republiky FV40187 (2019-2022) Optimalizace nových metod přípravy vysoce sofistikovaných krytů ran a jejich ověření pro použití především ve zdravotnictví
Ministerstvo průmyslu a obchodu České republiky FV40437 (2019-2022) Acti-TOX: Aktivní 3D kultivační systémy pro pokročilé toxikologické testování a redukci animálních experimentů
Ministerstvo zdravotnictví České republiky NV180500379 (2018 – 2021) Vývoj a komplexní hodnocení nové injekčně aplikovatelné, resorbovatelné, porézní kostní náhrady s řízeným uvolňováním antimikrobiálních
European Commission H2020-MSCA- RISE-2018, 8240072 (2019 – 2023) iP-OSTEO - Induced pluripotent stem cell seeded active osteochondral nanofibrous scaffolds
European Commission H2020-MSCA-RISE-2018, 823981 (2019 - 2023) ActiTOX - Active organotypic models for nanoparticle toxicological screening
Technologická agentura České republiky FW01010662 (2020 – 2024) Systémy řízeného dodávání léčiv pro léčbu osteoporotických defektů
Ministerstvo průmyslu a obchodu Program Aplikace CZ.01.1.02/0.0/0.0/17_107/0012524 (2018 – 2021) Vývoj produktů získaných zpracováním lidské kostní tkáně pro vybrané aplikace v tkáňovém inženýrství a regenerativní medicíně
Fakulta strojní, České vysoké učení technické v Praze
Fakulta chemické technologie, Vysoká škola chemicko-technologická v Praze
Lékařská fakulta Univerzity Karlovy v Plzni
Biomedicínské centrum Lékařské fakulty UK v Plzni
Vysoké učení technické v Brně, Fakulta chemická, Ústav chemie materiálů
Středoevropský technologický institut VUT (CEITEC), Pokročilé polymerní materiály a kompozity
Technická univerzita v Liberci
Inocure s.r.o., Česká republika
Corticalis AS, Norsko
Biofabics LDA, Portugalsko
Orthosera GmbH, Rakousko
Ospin GmbH, Německo
Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V., Německo
Instytut Podstawowych Problemów Techniki POLSKIEJ AKADEMII NAUK, Polsko
Scinus Cell Expansion bv, Nizozemsko
LLS Rowiak LaserLabSolutions GmbH, Německo
Hochschule Rhein-Waal (HSRW), Německo
University College London, Velká Británie
Szechenyi Istvan University, Maďarsko
BIONEER A/S, Dánsko
© Copyright 2018. All Rights Reserved. Stránky vytvořila agentura WebMotion.