Možná si to pamatujete z dětství: na zárubni dveří u vás doma byl tužkou nebo propisovačkou nalinkovaný žebříček vodorovných čar a u každé linky bylo připsáno datum a vaše jméno. Čím novější bylo datum, tím byla čára výše. Tento jednoduchý růstový graf zaznamenával vaši výšku v určitém věku a úsek, o jaký se změnila od posledního měření. Pravděpodobně jste brali jako samozřejmost, že jste rostli, každá novější linka byla výše než ta poslední, a nikdy vás asi ani nenapadlo zabývat se myšlenkou, proč tomu tak je.

Odchov bezmikrobních myší v plastovém izolátoru Trexler
V současnosti víme, že v juvenilním období růstu je velikost těla výsledkem interakce mezi příjmem živin a produkcí růstových hormonů v organismu. U savců je postnatální růst řízen činností tzv. somatotropní osy (schéma vpravo), ve které růstový hormon (growth hormone, GH), produkovaný hypofýzou, instruuje játra a periferní tkáně k tvorbě inzulinu podobnému růstovému faktoru 1 (insulin-like growth factor 1, IGF-1), který podporuje růst jednotlivých orgánů a také růst systémový. Většinu IGF-1, jenž se nachází v krevním oběhu, produkují játra; váže se na proteiny krevní plazmy, které prodlužují jeho životnost. Nejvýznamnějším z nich je IGF-vazebný protein 3 (insulin-like growth factor binding protein 3, IGFBP-3), jehož hladina je úměrná IGF-1 a nutričnímu stavu organismu. Faktor IGF-1, který produkují periferní orgány (svaly, chrupavky atd.) přispívá jen málo k celkovým hladinám v krevním oběhu a působí převážně autokrinně a parakrinně, což znamená, že působí zpětně na buňky (orgány), které jej produkují, nebo na buňky (orgány), jež s nimi sousedí. IGF-1 reguluje produkci GH tzv. negativní zpětnou vazbou, což znamená, že čím větší je koncentrace IGF-1 v plazmě, tím více je utlumena produkce GH.

V situacích, kdy je dlouhodobě málo potravy anebo strava neobsahuje dostatek živin (tzv. chronická podvýživa), se juvenilní růst zpomaluje. Zpomalování způsobuje míra odolnosti (rezistence) k působení GH, a tudíž tkáně přestávají reagovat na stimulaci GH. V důsledku toho klesá mj. produkce IGF-1, ztrácí se negativní zpětná vazba a nastává překvapivá situace: hladiny GH v plazmě se zvyšují, ale růst je zastaven. Pokles produkce IGF-1 má za následek opožděný vývoj a daný jedinec je menší a váží méně, než odpovídá jeho věku [viz Hizli et al., Pediatr Endocrinol Rev. Mar; 4(3):186–195, 2007]. V některých částech světa, jako jsou Afrika a Indie, je dětská podvýživa zásadním zdravotním problémem s dlouhodobými následky; kromě nízkého vzrůstu ji často doprovází deficit neurokognitivních funkcí.

Vědecké studie v poslední době ukázaly, že střevní mikrobiota hostitele hraje významnou roli pro fungování (fyziologii) živých organismů a pro procesy, které v nich nastávají. Chtěli jsme proto nalézt odpovědi na následující otázky: 1. Jakou roli hrají střevní bakterie v normálním postnatálním růstu? 2. Ovlivňují bakterie aktivitu somatotropní osy za podmínek nutričně dostatečné stravy a za podmínek chronické podvýživy?
Abychom nalezli odpověď na první otázku, použili jsme dvě skupiny myší: myši konvenční, tj. chované za normálních podmínek a kolonizované běžnou střevní mikroflórou, a myši bezmikrobní (axenické), které postrádají jakékoli detekovatelné živé mikroorganismy (Box Gnotobiologie). Mladé myši byly po odstavení převedeny na běžnou potravu s potřebnými živinami v dostatečném množství; jejich růst, váhový i délkový, jsme sledovali až do dospělosti. Konvenční myši vykazovaly vyšší rychlost růstu a jejich konečná hmotnost a délka byly větší ve srovnání s myšmi bezmikrobními. Pozorovaný rozdíl nezpůsobily větší tukové zásoby, nýbrž vyšší hmotnost vnitřních orgánů a lepší růst kostí. Kromě těchto makroskopických rozdílů jsme také zjistili, že přítomnost střevní mikrobioty zlepšila funkci somatotropní osy a zvedla hladinu IGF-1 v séru konvenčních myší. Po zjištění, že přítomnost bakterií je pro optimální růst nezbytná, jsme chtěli vědět, zda bakterie hrají stejnou roli i za podmínek chronické podvýživy. Abychom navodili takové podmínky, navrhli jsme dietu chudou na bílkoviny, tuky a vitaminy. Bezmikrobní mladé myši, které jsme na tuto dietu převedli, přestaly růst do délky a přibývat na váze – jejich růst se úplně zastavil. Na druhou stranu, jejich konvenční protějšky v růstu pokračovaly, i když pomaleji než konvenční myši krmené běžnou potravou; opět jsme pozorovali, že střevní mikrobiota zlepšila fungování somatotropní osy, což doprovázely vyšší hladiny IGF-1 a IGFBP-3 v séru.
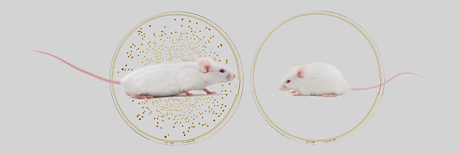
Střevní bakterie jsou u myší nezbytné pro optimální postnatální růst a přispívají k určení finální velikosti dospělých jedinců.
Pokud jde o růst hostitelského organismu a bakteriální kolonizaci, tým dr. Françoise Leuliera z Institutu funkční genomiky v Lyonu ve Francii prokázal, že některé specifické bakterie druhu Lactobacillus (L.) plantarum jsou schopné podporovat růst larev octomilky (Drosophila melanogaster), které se vyvíjejí na dietě s nedostatkem proteinů [viz Storelli et al., Cell Metab 14(3):403–414, 2011]. L. plantarum patří mezi bakterie mléčného kvašení, které díky jejich adaptabilitě můžeme nalézt ve variabilních biotopech, jako jsou zelenina, půda a mléčně kvašené potraviny, ale také v zažívacím traktu bezobratlých a obratlovců včetně myší a lidí. Octomilky náleží mezi hmyz s dokonalou proměnou (holometabola); z vajíčka se líhne larva, která během krátké doby zvětší svou váhu stokrát a svou délku šestkrát a následně se zakuklí – za ideálních podmínek během asi pěti dní. Když jsou však vystaveny dietě s nedostatkem proteinů, doba se prodlužuje na osm dní; pokud jsou této dietě vystaveny bezmikrobní larvy octomilek, je doba ještě delší. Kolonizujeme-li bezmikrobní larvy bakterií L. plantarum, která se běžně vyskytuje ve střevu octomilek, larvální stadium se zkrátí na stejnou dobu, kterou potřebují k zakuklení larvy konvenční, tedy asi osm dní. Tato schopnost byla kmenově specifická, což znamená, že různé kmeny L. plantarum se lišily v efektivitě, s jakou byly schopny růst larev podporovat.

Schematické znázornění somatotropní osy
Položili jsme si otázku, zda je jediná bakterie, která podporuje růst modelového bezobratlého organismu, schopna podporovat růst také v myším modelu chronické podvýživy – a do jaké míry? Za tímto účelem jsme monokolonizovali původně bezmikrobní myši kmenem L. plantarum WJL, jenž podporoval růst v muším modelu, a další skupinu myší jsme osadili kmenem L. plantarum NIZO2877; ten takovou schopnost podporovat růst larev neměl. Po převedení na experimentální chudou dietu myši osazené kmenem L. plantarum WJL rostly a na konci pokusu vážily a měřily stejně jako konvenční myši na této dietě. Naproti tomu myši osazené kmenem L. plantarum NIZO2877 rostly mnohem méně. L. plantarum WJL také dokázal zlepšit funkci somatotropní osy ve stejném rozsahu, jak jsme pozorovali u konvenčních myší, kdežto myši osazené L. plantarum NIZO2877 se v tomto ohledu více podobaly myším bezmikrobním.
Na myším modelu se nám podařilo prokázat [viz Schwarzer et al., Science 351(6279):854–857, 2016], že střevní mikrobiota je nezbytná a některé vybrané kmeny bakterie L. plantarum jsou dostatečné ke zlepšení činnosti somatotropní osy pro zlepšení juvenilního růstu za podmínek chronické podvýživy. Přestože prozatím nevíme, zda mechanismus, kterým L. plantarum podporuje juvenilní růst u myši a mouchy je stejný, výsledky ukazují, že by mohlo jít o vlastnost, jež je zachována v živočišné říši, a tudíž by mohla fungovat i u lidí. Domníváme se, že spolu s re-nutričními strategiemi tak může podávání vybraných kmenů bakterií představovat novou a doplňkovou cestu, jež má šanci zmírnit nepříznivé účinky chronické podvýživy, kterou v rozvojových zemích trpí více než 160 milionů dětí do pěti let, na postnatální růst.
MARTIN SCHWARZER a HANA KOZÁKOVÁ,
Laboratoř gnotobiologie,
Mikrobiologický ústav AV ČR, v. v. i.
O mouchách a myších
V dubnu 2010 způsobil výbuch vulkánu Eyjafjallajökull výpadek v letecké dopravě v celé Evropě. Tehdy se ve španělském San Feliu de Guixol uskutečnila ESF-EMBO konference, na kterou se dostavili jen přednášející, kteří se rozhodli cestovat po souši – z nemnoha účastníků právě dr. François Leulier, který v té době dokončoval práci o efektu bakterií Lactobacillus (L.) plantarum na růst larev mouchy octomilky (Drosophila melanogaster) za podmínek proteinové nutriční podvýživy. Další účastnicí byla vedoucí laboratoře gnotobiologie v Novém Hrádku dr. Hana Kozáková, jejíž tým pracoval na prevenci vývoje alergií u myší monokolonizovaných právě bakterií L. plantarum. Konference se konala v uvolněném duchu, a protože mnohé přednášky kvůli nepřítomnosti přednášejících odpadly, diskutovali účastníci své vědecké projekty a zájmy více do detailů. Při jedné z diskusí s dr. F. Leulierem uvedla dr. H. Kozáková, že by bylo podnětné zjistit, zda by bakterie L. plantarum, která podporuje růst v muším modelu, fungovala i u savců, tedy například v myším modelu. Slovo dalo slovo a zrodila se spolupráce, která stále úspěšně pokračuje
Gnotobiologie je vědní disciplína studující živočišné organismy získané aseptickými chirurgickými postupy nebo sterilním vylíhnutím z vajec (a dále chované ve sterilních izolátorech a krmené sterilní potravou), jež jsou buď bezmikrobní (axenické, angl. germ-free), nebo osazené definovanými bakteriemi. Výraz gnotobiologie je složenina dvou řeckých slov: gnotos (známý) a bios (život). Laboratoř gnotobiologie v Dolech u Nového Hrádku (okres Náchod) je součástí Mikrobiologického ústavu AV ČR a je jednou z mála evropských laboratoří s dlouhodobou tradicí v chovu a studiu bezmikrobních zvířat. Její historie započala již roku 1953. V prostorách původní textilní továrny vznikla stanice Biologického ústavu ČSAV, která se zpočátku zabývala infekční mikrobiologií. V roce 1960 byla přebudována na laboratoř gnotobiologickou, v níž pod vedením imunologa světového významu prof. Jaroslava Šterzla založili Ing. Leoš Mandel a Ing. Jiří Trávníček odchov bezkolostrálních bezmikrobních selat. Zásluhou dr. Renaty Štěpánkové byly do bezmikrobních podmínek převedeny další modelové organismy – potkani, králíci a myši.


 English
English

















